Olumiant (Baricitinib), thuốc nhắm mục tiêu trong điều trị viêm khớp dạng thấp
1. Khái niệm hệ Tyrosine Kinase và Janus Kinase
1.1. Tyrosine Kinase
Trong hóa sinh, kinase là một dạng enzyme có chức năng chuyển nhóm phosphate từ các phân tử cao năng lượng (ATP) tới một phân tử đích là protein đặc hiệu. Quá trình này gọi là sự phosphoryl hóa protein. Ngược lại các phosphatase là các enzyme gỡ nhóm phosphate này ra khỏi phân tử protein.
Enzyme kinase đặc hiệu cho việc chuyển nhóm phosphate của các phân tử cao năng cho các acid amin Tyrosines được gọi là Tyrosine kinases.
Tyrosine kinase là một enzyme có chức năng chuyển một nhóm phosphate từ ATP sang acid amin Tyrosine ở phân tử protein trong tế bào. Nó hoạt động như một công tắc “bật” hoặc “tắt” trong nhiều chức năng. Nhóm phosphat được gắn vào acid amin tyrosine trong phân tử protein làm phân tử protein này được phosphoryl hóa. Tyrosine kinase là một nhóm nhỏ của lớp protein kinase, lớp protein kinase này ngoài việc phosphoryl hóa các protein có Tyrosine, nó còn phosphoryl hóa các phân tử protein có các axit amin khác như serine và threonine. Phosphryl hóa protein bởi kinase là một cơ chế quan trọng trong việc truyền tín hiệu trong một tế bào và điều chỉnh hoạt động của tế bào, chẳng hạn như phân chia và tăng trưởng tế bào.
1.2. Janus Kinase
Janus kinase (Jak) là một trong mười họ tyrosine kinase không thụ thể, nội bào, truyền tín hiệu qua trung gian cytokine thông qua con đường JAK-STAT. Chúng được phát hiện trong khi tìm kiếm các tyrosine kinase protein mới bằng cách sử dụng các chiến lược dựa trên PCR hoặc lai độ nghiêm ngặt thấp. Ban đầu chúng được đặt tên là "chỉ khác kinase" 1 và 2, nhưng cuối cùng được gọi là "Janus kinase". Mô hình tín hiệu JAK – STAT được phát hiện cách đây hai thập kỷ, cung cấp một bước đột phá trong sự hiểu biết về sinh học cytokine.
Ở người, gen Jak1 nằm trên nhiễm sắc thể 1p31.3 và Jak2 nằm trên 9p24; các gen Jak3 và Tyk2 được tập hợp lại với nhau trên nhiễm sắc thể 19p13.1 và 19p13.2.
Các JAK có kích thước từ 120-140 kDa và có bảy vùng tương đồng xác định được gọi là miền tương đồng Janus từ 1 đến 7 (JH1-7). JH1 là miền kinase quan trọng đối với hoạt động enzym của JAK và chứa các đặc điểm điển hình của kinase tyrosine như các tyrosine được bảo tồn cần thiết để kích hoạt JAK. Sự phosphoryl hóa của các tyrosine kép này dẫn đến những thay đổi cấu trúc trong protein JAK để tạo điều kiện liên kết cơ chất. JH2 là một "miền pseudokinase", một miền có cấu trúc tương tự như tyrosine kinase và cần thiết cho hoạt động kinase bình thường, nhưng thiếu hoạt động của enzym. Miền này có thể tham gia vào việc điều hòa hoạt động của JH1, và có thể là sự sao chép của miền JH1 đã trải qua quá trình nhân đôi đột biến.
Đầu cuối amin (NH2) kết thúc (JH4-JH7) của Jaks được gọi là miền FERM (viết tắt của dải 4,1 ezrin, radixin và moesin); miền này cũng được tìm thấy trong họ kinase bám dính khu trú (FAK) và có liên quan đến sự liên kết của các JAK với các thụ thể cytokine và/hoặc các kinase khác.
Các chất sau khi gắn với receptor trên màng tế bào có thể làm hoạt hoá con đường dẫn truyền thông tin nội tế bào qua 3 cách: thông qua protein G, qua kênh ion hoặc qua liên kết enzyme tyrosin kinase. JAK là 1 trong 10 họ của tyrosin kinase, đây là protein đóng vai trò quan trọng trong dẫn truyền nội bào của các cytokin (con đường JAK – STAT).
Các cytokin bao gồm interleukin, interferon và các phân tử khác gắn với receptor sẽ làm hoạt hoá protein JAK nội bào sau đó làm protein STAT được phosphoryl hoá và dimer hoá rồi di chuyển đến nhân để trực tiếp điều hoà bộc lộ gen. Có thể nói JAK – STAT là con đường tín hiệu nội bào mà tại đó nhiều tín hiệu tiền viêm hội tụ lại với nhau.
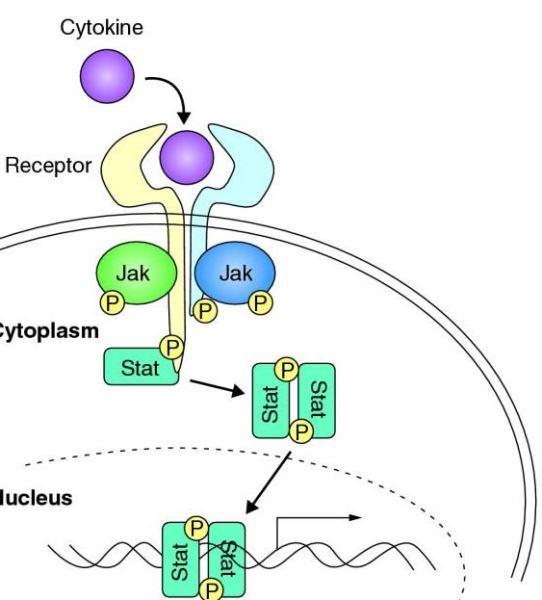
Hình 1. Sơ đồ mô tả con đường JAK – STAT.
Tổng quan về tín hiệu cytokine. Các cytokine liên kết với các thụ thể homodimeric hoặc dị phân tử, các thụ thể này được cấu thành liên kết với Jaks. Các Jaks được cho là được kích hoạt bởi sự thay đổi cấu trúc trong thụ thể cho phép chuyển hóa và / hoặc tự động phosphoryl hóa hai Jaks liên kết. Các chất này lần lượt phosphoryl hóa các thụ thể cytokine. Các protein Stat liên kết các chuỗi thụ thể đã được phosphoryl hóa, cho phép các Jaks phosphoryl hóa các Thống kê. Số liệu thống kê được phosphoryl hóa tạo thành dimer và chuyển vị trí và tích lũy trong nhân, nơi chúng điều chỉnh sự biểu hiện gen.
Hiện tại vẫn chưa rõ cấu trúc ba chiều của Jaks ở người. Một phần vì chúng là những protein tương đối lớn gồm hơn 1.100 acid amin, với khối lượng phân tử biểu kiến là 120-140 kDa. Từ cấu trúc sơ cấp, cấu trúc miền giả định đã được công nhận là được bảo tồn giữa các loài động vật có vú, gia cầm, teleost và côn trùng. Bảy miền tương đồng Jak (JH) đã được xác định, được đánh số từ cacboxyl đến đầu cuối amin.
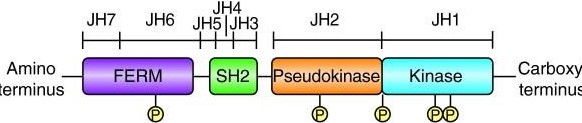
Hình 2. Biểu diễn giản đồ về cấu trúc chính của Janus kinase (Jaks), được tạo thành từ các miền FERM, giống SH2, pseudokinase và kinase. Một danh pháp thay thế cho các miền giả định là một loạt các miền tương đồng Janus (JH). Miền FERM làm trung gian liên kết với các thụ thể cytokine. Cả miền FERM và miền pseudokinase điều chỉnh hoạt tính xúc tác và dường như tương tác với miền kinase. Jaks autophosphorylate tại nhiều vị trí (P), bao gồm cả hai trong vòng lặp kích hoạt của miền kinase, nhưng chức năng chính xác của những sửa đổi này chỉ mới bắt đầu được hiểu.
Ở động vật có vú có bốn thành viên trong họ này là Jak1, Jak2, Jak3 và Tyrosine kinase 2 (Tyk2). Bốn thành viên gia đình JAK là:
- Janus kinase 1 (JAK1)
- Janus kinase 2 (JAK2)
- Janus kinase 3 (JAK3)
- Tyrosine kinase 2 (TYK2)
JAK nằm ở phía bào tương của các receptor của cytokine type I và II. Dẫn truyền tín hiệu khi các cytokine này gắn với các receptor tương thích. JAK kích hoạt chất dẫn truyền tín hiệu và yếu tố sao chép trong tế bào (STATs)
Ở động vật có vú, Jak1, Jak2 và Tyk2 được biểu hiện khắp nơi. Ngược lại, biểu hiện của Jak3 bị hạn chế hơn; nó chủ yếu được biểu hiện trong các tế bào tạo máu và được điều chỉnh rất nhiều với sự phát triển và hoạt hóa của tế bào. Mối liên hệ giữa Jaks và tín hiệu cytokine lần đầu tiên được tạo ra bằng cách sử dụng các dòng tế bào đột biến thiếu khả năng đáp ứng với interferon (IFN). Một dòng tế bào như vậy được chứng minh là thiếu Tyk2 và việc thêm lại tín hiệu IFN đã khôi phục kinase này.
Mỗi protein có miền kinase và miền pseudo-kinase không hoạt động về mặt xúc tác, và chúng liên kết với các thụ thể cytokine thông qua các miền FERM ở đầu tận cùng. Khi liên kết các cytokine với các thụ thể của chúng, Jaks được kích hoạt và phosphoryl hóa các thụ thể, tạo ra các vị trí gắn kết cho các phân tử tín hiệu, đặc biệt là các thành viên của bộ chuyển tín hiệu và chất kích hoạt họ phiên mã (Stat). Thông qua việc tạo ra các dòng tế bào thiếu Jak ở chuột nhắm mục tiêu gen, các chức năng thiết yếu của Jaks trong việc truyền tín hiệu cytokine đã được thiết lập. Điều quan trọng là, sự thiếu hụt Jak3 là cơ sở của suy giảm miễn dịch kết hợp trầm trọng autosomal ở người (SCID); theo đó, một chất ức chế Jak3 có chọn lọc đã được phát triển, tạo thành một nhóm thuốc ức chế miễn dịch mới.
- Một số lượng lớn các cytokine phụ thuộc vào Jak1, bao gồm một họ sử dụng tiểu đơn vị thụ thể chung được gọi là chuỗi γ chung (γc), bao gồm interleukin (IL) như IL-2, IL-4, IL-7, IL-9, IL-15 và IL-21. Các cytokine này cũng phụ thuộc vào Jak3, vì Jak3 liên kết với γc. Jak1 cũng cần thiết cho một gia đình khác sử dụng tiểu đơn vị thụ thể chung gp130 (IL-6, IL-11, oncostatin M, yếu tố ức chế bệnh bạch cầu (LIF), yếu tố nuôi dưỡng thần kinh thể mật (CNF)) cũng như yếu tố kích thích thuộc địa tế bào hạt (G -CSF) và IFN. Ở chuột loại trực tiếp Jak1 có kiểu hình gây chết chu sinh, do liên quan đến các khuyết tật thần kinh khiến chúng không thể bú sữa. Những con chuột này cũng có chức năng và sự phát triển tế bào lympho bị khiếm khuyết do tín hiệu bị lỗi của các cytokine thông qua Jak1.
- Jak2 cần thiết cho các cytokine giống hormone như hormone tăng trưởng (GH), prolactin (PRL), erythropoietin (EPO), thrombopoietin (TPO) và họ các cytokine phát tín hiệu qua thụ thể IL-3 (IL-3, IL -5 và yếu tố kích thích thuộc địa bạch cầu hạt-đại thực bào, GM-CSF). Jak2 cũng quan trọng đối với các cytokine sử dụng thụ thể gp130 và đối với một số IFN. Sự hòa hợp gen JAK2 với gen TEL(ETV6) (TEL-JAK2) và PCM1 được tìm thấy ở những bệnh nhân mắc leukemia, đặc biệt là leukemia dòng bạch cầu ái toan. Đột biến Jak-2 kinase có mối tương quan cao với những bất thường tim bẩm sinh ở vùng Nam Á mang gen PYFA. Các đột biến ở JAK2 liên quan với bệnh đa hồng cầu nguyên phát, tăng tiểu cầu nguyên phát, và myelofibrosis cũng như các rối loạn sinh tủy khác. Xác định được đột biến Jak2 là một trong những phương pháp chẩn đoán đa hồng cầu nguyên phát. Ở Chuột thiếu Jak2 dẫn đến chết phôi ở ngày phôi 12,5 do thất bại trong quá trình tạo hồng cầu.
- Thiếu hụt Jak3 lần đầu tiên được xác định ở người bị suy giảm miễn dịch kết hợp trầm trọng thể lặn (SCID). Bây giờ chúng ta biết rằng Jak3 liên kết với γc và sự thiếu hụt Jak3 hoặc γc sẽ làm giảm tín hiệu của họ các cytokine sử dụng tiểu đơn vị thụ thể này. Điều này gây ra những hậu quả nghiêm trọng về mặt phát triển và chức năng của tế bào miễn dịch. Cùng với đột biến ở thụ thể IL-7, γc và Jak3 chiếm 2/3 đến 3/4 trường hợp SCID.
Những con chuột chuyển gen không biểu hiện JAK1 có phản ứng khiếm khuyết với một số cytokine, chẳng hạn như interferon-gamma . JAK1 và JAK2 tham gia vào tín hiệu interferon loại II (interferon-gamma), trong khi JAK1 và TYK2 tham gia vào tín hiệu interferon loại I. Những con chuột không biểu hiện TYK2 có chức năng tế bào tiêu diệt tự nhiên bị lỗi.
Vì các thành viên của họ thụ thể cytokine loại I và loại II không có hoạt tính kinase xúc tác, chúng dựa vào họ tyrosine kinase thuộc họ JAK để phosphoryl hóa và kích hoạt các protein hạ lưu liên quan đến con đường dẫn truyền tín hiệu của chúng. Các thụ thể tồn tại dưới dạng polypeptit bắt cặp, do đó thể hiện hai miền truyền tín hiệu nội bào.
Một số ví dụ về các phân tử sử dụng con đường tín hiệu JAK / STAT là yếu tố kích thích khuẩn lạc, prolactin, hormone tăng trưởng và nhiều cytokine .
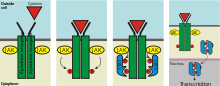
Hình 3. Hoạt động sinh học của JAK. Hệ thống JAK-STAT bao gồm ba thành phần chính: (1) một thụ thể (màu xanh lá cây), xuyên qua màng tế bào; (2) Janus kinase (JAK) (màu vàng), được liên kết với thụ thể, và; (3) Bộ truyền tín hiệu và chất kích hoạt phiên mã (STAT) (màu xanh lam), mang tín hiệu vào nhân và DNA. Các chấm đỏ là phốt phát. Sau khi cytokine liên kết với thụ thể, JAK sẽ thêm một phosphate vào (phosphorylat) thụ thể. Điều này thu hút các protein STAT, chúng cũng được phosphoryl hóa và liên kết với nhau, tạo thành một cặp (dimer). Dimer di chuyển vào nhân, liên kết với DNA và gây ra quá trình phiên mã gen. Các enzym bổ sung các nhóm photphat được gọi là protein kinaza.
2. Thuốc nhắm mục tiêu Janus kinase
Thuốc ức chế JAK hay còn gọi là jakinib là các phân tử nhỏ chỉ khoảng 400kDa có thể dễ dàng xâm nhập vào bên trong tế bào để ức chế phân tử JAK. Thuốc gồm 2 thế hệ, trong đó thế hệ 1 được nghiên cứu nhiều nhất. Hiện nay một số loại thuốc jakinib thế hệ 1 cũng đã có mặt tại thị trường Việt Nam.
Bảng 1. Các thuốc ức chế Janus Kinase đã được FDA chấp thuận
|
Thuốc |
FDA chấp thuận |
|
Tofacitinib |
Là thuốc đầu tiên được FDA chấp thuận để điều trị: Viêm khớp dạng thấp (2012) Viêm khớp vảy nến (2017) Viêm loét đại tràng (2018)
|
|
Ruxolitinib |
Bệnh xơ tuỷ (2011) Đa hồng cầu nguyên phát (2014) |
|
Baricitinib |
Viêm khớp dạng thấp (2018) Nghiên cứu pha 2 vảy nến và viêm da cơ địa |
|
Oclacitinib |
Chưa được chấp thuận ở người Viêm da cơ địa ở chó |
JAK1, JAK3 và STAT 6 (signal transducer and activator of transcription) là trung gian cho tín hiệu IL-4, và đây là mục tiêu điều trị tiềm năng của AD (Atopic Dermatitis: chàm thể tạng). Ức chế JAK 1, JAK 3 sẽ làm giảm tín hiệu IL-4, qua đó giảm đáp ứng miễn dịch của Th2 và làm cải thiện triệu chứng của chàm thể tạng.
Tofacitinib citrate: chất ức chế JAK1, JAK3. Thuốc được chấp thuận trong điều trị viêm khớp dạng thấp trung bình - nặng. Gần đây được chứng minh có hiệu quả trong điều trị rụng tóc từng vùng, yếu tố thường kết hợp với chàm thể tạng (AD).
Cuối cùng là Jak3, vì vai trò quan trọng của Jak3 trong việc truyền tín hiệu cytokine thông qua γc và vì sự biểu hiện ở mô hạn chế của nó, việc ức chế hoạt động của Jak3 đã nổi lên như một chiến lược đầy hứa hẹn để ức chế miễn dịch. Một chất ức chế Jak3 có tính chọn lọc cao và mạnh (CP-690, 550) gần đây đã được phát triển có hiệu lực nano đối với Jak3 trong ống nghiệm , với hiệu lực kém hơn nhiều so với các thành viên khác trong gia đình Jak. Do đó, CP-690, 550 đều rất hiệu quả và được dung nạp tốt trong các mô hình cấy ghép nội tạng động vật. Người ta có thể dự đoán rằng loại thuốc này sẽ giúp khắc phục những tác dụng phụ không đáng có thường thấy ở những bệnh nhân đang điều trị bằng thuốc ức chế miễn dịch. Do đó, thuốc có thể hữu ích trong việc ngăn chặn thải ghép và điều trị các bệnh tự miễn dịch. Có thể hình dung, nó cũng có thể hữu ích trong việc điều trị những khối u ác tính huyết học có biểu hiện kích hoạt Jak3.
Nhắm mục tiêu Tyk2 với các loại thuốc cụ thể cũng sẽ hợp lý, do vai trò hạn chế của nó; có lẽ chất ức chế Tyk2 sẽ hữu ích trong một số bệnh qua trung gian miễn dịch. Liệu một chất ức chế Jak2 có hữu ích trong các khối u ác tính hay không cũng đáng được xem xét.
3. Các thuốc ức chế cytokin mới được đưa vào điều trị viêm khớp dạng thấp
Các thuốc mới đây được đưa vào điều trị viêm khớp dạng thấp chủ yếu chống lại hoạt động của hệ miễn dịch một cách không điển hình. Có hai loại đó là: liệu pháp sinh học nhắm vào những yếu tố được cho là nguyên nhân gây viêm và phá hủy khớp, và các thuốc nhắm mục tiêu là các thuốc nhắm vào những phân tử nhất định của chuỗi bệnh lý.
Trong số các thuốc sinh học thì thuốc kháng TNF được sử dụng nhiều nhất, gồm 5 loại là infliximab (Remicade®), etanercept (Enbrel®), adalimumab (Humira®), certolizumab (Cimzia®) và golimumab (Simponi®). Mời đọc thêm bài: http://hahoangkiem.com/thuoc/enbrel-entanercep-thuoc-sinh-hoc-moi-dieu-tri-viem-khop-dang-thap-1535.html
Các thuốc nhắm mục tiêu hiện nay có hai thuốc đã được FDA phê duyệt là Xeljanz (tofacitinib) và Olumiant (baricitinib).
Tác dụng phụ điển hình nhất của thuốc ức chế cytokin là gây giảm miễn dịch đối với một số loại viêm nhưng thuốc cho hiệu quả rất tốt và là cuộc cách mạng trong điều trị bệnh viêm khớp dạng thấp. Bệnh nhân không còn đau, viêm và biến dạng khớp.
3.1. Thuốc Xeljanz (tofacitinib)
Tofacitinib là chất ức chế JAK đầu tiên được FDA phê chuẩn vào năm 2012 đối với người lớn bị viêm khớp dạng thấp từ trung bình đến nặng, có đáp ứng không đầy đủ với methotrexate. Có bốn enzyme JAK: JAK1, JAK2, JAK3 và Tyk2. Xeljanz chủ yếu ức chế JAK1 và JAK3, và nó được uống hai lần mỗi ngày.
3.2. Thuốc Olumiant (baricitinib)
Baricitinib là một loại thuốc điều trị viêm khớp dạng thấp (RA) nhắm mục tiêu ngăn chặn Janus kinase (JAK), JAK là một nhóm các enzyme kích hoạt các tín hiệu viêm bên trong tế bào. Đây là thuốc thứ hai trong nhóm thuốc này được tung ra thị trường để điều trị viêm khớp dạng thấp. Trước đó tofacitinib (Xeljanz) là thuốc đầu tiên được chấp thuận vào năm 2012.
Ngày 1/6/2018, FDA đã phê duyệt Olumiant (baricitinib) được dùng điều trị viêm khớp dạng thấp cho người trưởng thành có mức độ bệnh từ trung bình đến nặng, có đáp ứng không đầy đủ với một hoặc nhiều liệu pháp ức chế hoại tử khối u (TNF).
Đây không phải là một tác nhân sinh học mà là một "phân tử nhỏ", hay thuốc uống, nhắm mục tiêu, có hiệu quả cao trong điều trị các dấu hiệu và triệu chứng của viêm khớp dạng thấp (RA). Nó được dự kiến sẽ rẻ hơn đáng kể so với thuốc sinh học.
Baricitinib là một chất ức chế Janus kinase 1 (JAK1) và 2 (JAK2) chọn lọc và có thể đảo ngược. Janus kinase thuộc họ tyrosine protein kinase và đóng một vai trò quan trọng trong quá trình truyền tín hiệu tiền viêm thường được kích hoạt quá mức trong các rối loạn tự miễn dịch như viêm khớp dạng thấp. Bằng cách chặn các hành động của JAK1 / 2, baricitinib phá vỡ sự kích hoạt các phân tử tín hiệu xuôi dòng và các chất trung gian gây viêm. Viêm khớp dạng thấp là một bệnh tự miễn tiến triển gây tổn thương khớp. Trong suốt quá trình tiến triển của bệnh, căn bệnh này có thể dẫn đến sự xói mòn và biến dạng khớp, gây tử vong sớm, suy giảm chức năng và giảm chất lượng cuộc sống. Mặc dù có một số loại thuốc (DMARDs) có sẵn để điều trị, bệnh nhân thường gặp phải sự phản ứng không hợp lý đối với các thuốc này. Trong các mô hình động vật của viêm khớp, baricitinib đã được chứng minh là có tác dụng chống viêm đáng kể, nhưng cũng dẫn đến việc bảo tồn sụn và xương, không có sự ức chế miễn dịch dịch thể hoặc tác dụng huyết học bất lợi. Vào tháng 2 năm 2017, Baricitinib đã được chấp thuận sử dụng ở EU như một liệu pháp uống thứ hai trong điều trị viêm khớp dạng thấp hoạt động từ trung bình đến nặng ở người lớn, một mình hoặc kết hợp với methotrexate. Nó được bán trên thị trường dưới tên thương mại Olumiant. Tháng 6/2018, FDA đã phê duyệt cho sử dụng thuốc này để điều trị những trường hợp bệnh trung bình và nặng nhưng đáp ứng không đầy đủ với liệu pháp ức chế TNF. Trong khi Xeljanz (tofacitinib) chủ yếu ức chế JAK1 và JAK3 thì aricitinib ức chế JAK1 và JAK2 và được uống mỗi ngày một lần 2mg.
- Cơ chế hoạt động:
JAK là một thành phần của họ tyrosine kinase liên kết ở vùng nội bào của các thụ thể cytokine, thúc đẩy các tầng tín hiệu của cytokine và các yếu tố tăng trưởng liên quan đến bệnh lý tạo máu, viêm và chức năng miễn dịch, viêm khớp. Các cytokine tiền viêm lưu hành liên kết với các thụ thể bề mặt tế bào. Sau khi liên kết các cytokine ngoại bào và các yếu tố tăng trưởng, JAK được phosphoryl hóa, kích hoạt các bộ chuyển đổi tín hiệu và kích hoạt phiên mã (STAT). Thông qua các tầng tín hiệu, sự sao chép cytokine và chemokine gây viêm được tạo ra để tạo thành các chất trung gian gây viêm bao gồm IL-2, IL-6, IL-12, IL-15, IL-23, IFN-và GM-CSF. Baricitinib chọn lọc và đảo ngược ức chế JAK1 và JAK2 để điều chỉnh đường dẫn tín hiệu của chúng, do đó làm giảm quá trình phosphoryl hóa và giảm kích hoạt STATs, kết quả là làm giảm sự tạo thành các IL gây viêm. Trong các xét nghiệm enzyme phân lập, baricitinib cũng thể hiện tác dụng ức chế đối với các loại enzyme JAK khác, Tyrosine Kinase2 và JAK3, ở nồng độ cao hơn cần thiết cho sự ức chế JAK1/2.
Các chất ức chế JAK là một loại DMARDS thứ ba, được gọi là DMARDS phân tử nhỏ. Sự sẵn có của baricitinib sẽ cung cấp thêm một lựa chọn điều trị cho bệnh viêm khớp dạng thấp. Những bệnh nhân có đáp ứng không đầy đủ với methotrexate, DMARD khác hoặc thuốc sinh học, sau đó sẽ có một loại thuốc uống khác như một lựa chọn. Đối với một số bệnh nhân, nó có thể là một lựa chọn thuận tiện hơn và tốt hơn là dùng thuốc sinh học tự tiêm hoặc thuốc sinh học được tiêm truyền.
- Chuyển hóa thuốc:
Baricitinib trải qua quá trình oxy hóa bởi CYP3A4, mặc dù ít hơn 10% tổng liều dễ bị biến đổi sinh học này. Không có sự hình thành các chất chuyển hóa có thể định lượng trong huyết tương.
Thuốc được chuyển hóa ở gan bằng CYP3A4 và CYP2C19. Các chất chuyển hóa được tạo ra là các chất không hoạt động.
- Tính an toàn:
Nhà sản xuất Baricitinib Eli Lilly và Company đã tìm kiếm sự chấp thuận cho cả liều 2 mg và liều 4 mg, nhưng FDA đã phê duyệt vào năm 2018 chỉ với liều 2 miligam (mg). Cơ quan này bày tỏ lo ngại về các trường hợp huyết khối tĩnh mạch sâu (DVT) trong các thử nghiệm lâm sàng ở bệnh nhân dùng liều 4 mg. Huyết khối tĩnh mạch sâu là cục máu đông hình thành trong tĩnh mạch sâu, thường ở chân. Nó có thể gây sưng, đỏ và đau, và có thể vỡ ra và di chuyển đến phổi, có thể gây tử vong.
Baricitinib sẽ được cảnh báo (đóng khung) về nguy cơ huyết khối (cục máu đông) cũng như nhiễm trùng và khối u ác tính nghiêm trọng. Đối thủ cạnh tranh chính của nó, tofacitinib (cũng được chấp thuận ở mức thấp hơn hai liều mà nó áp dụng), mang một cảnh báo đóng khung tương tự, trừ cảnh báo huyết khối.
- Độc tính:
Dữ liệu phi lâm sàng cho thấy không có mối nguy hiểm đặc biệt nào đối với con người dựa trên các nghiên cứu thông thường về độ an toàn dược lý, độc tính gen và khả năng gây ung thư. Mặc dù vậy bariticinib đã cho thấy làm giảm số lượng tế bào lympho, bạch cầu ái toan và basophils cũng như sự suy giảm lympho trong các cơ quan / mô của hệ thống miễn dịch ở chuột và chó. Nhiễm trùng cơ hội liên quan đến demodicosis (mange) đã được quan sát thấy ở những con chó ở mức phơi nhiễm khoảng 7 lần so với phơi nhiễm ở người. Với liều khoảng 6-36 lần so với liều chỉ định ở người, giảm tế bào hồng cầu đã được quan sát thấy ở chuột và chó. Trong các nghiên cứu độc tính sinh sản của chuột và thỏ, baricitinib đã được chứng minh là làm giảm sự tăng trưởng / trọng lượng của thai nhi và tạo ra dị tật về xương (ở mức phơi nhiễm tương ứng khoảng 10 và 39 lần so với con người). Baricitinib làm giảm khả năng sinh sản và các chỉ số thụ thai trong một nghiên cứu sinh sản chuột đực / cái kết hợp. Giảm hiệu suất tổng thể có khả năng là do chức năng sinh sản của chuột cái bị thay đổi, vì không có thay đổi có thể phát hiện được về sinh tinh trùng hoặc tinh dịch / điểm cuối tinh trùng ở chuột đực. Ở chuột cái, đã giảm số lượng lutea và vị trí cấy, giảm mất trước khi cấy và / hoặc ảnh hưởng xấu đến sự tồn tại trong tử cung của phôi. Trong một nghiên cứu phát triển trước và sau khi sinh của chó, đã giảm trọng lượng của trẻ khi tiếp xúc gấp 4 lần phơi nhiễm ở người và giảm tỷ lệ sống sau sinh sau khi tiếp xúc với 21 lần phơi nhiễm ở người. Baricitinib được phát hiện trong sữa của những con chuột đang cho con bú. Sự liên quan lâm sàng ở người chưa được thiết lập. Tất cả các phản ứng bất lợi liên quan đến baricitinib dự kiến sẽ xảy ra phụ thuộc vào liều.
- Tác dụng phụ:
+ Huyết học: Thường gặp: Tăng tiểu cầu , thiếu máu. Không phổ biến (0,1% đến 1%): Giảm bạch cầu (gặp 1% đến 10%). Tần suất không được báo cáo: L lymphocytosis (xảy ra với tỷ lệ cao hơn ở người cao tuổi).
+ Miễn dịch học: Thường gặp: Herpes zoster, herpes simplex (ví dụ: eczema herpeticum, herpes simplex, ophthalmic herpes simplex, herpes miệng), cúm (gặp 1% đến 10%).
+ Cơ xương khớp: Thường gặp: Đau khớp, viêm khớp dạng thấp, đau lưng , co thắt cơ, đau cơ (gặp 1% đến 10%).
+ Mắt: Thường gặp: Mờ mắt (1% đến 10%). Không phổ biến: Đục thủy tinh thể (0,1% đến 1%).
+ Chuyển hóa: Rất phổ biến: Tăng cholesterol máu (34%).
Không phổ biến: Tăng triglyceride máu, tăng cân, creatine phosphokinase tăng lên hơn 5 lần giới hạn trên của mức bình thường (0,1% đến 1%).
+ Tâm thần: Không phổ biến: Mất ngủ , trầm cảm (gặp 0,1% đến 1%).
+ Bộ phận sinh dục: Thường gặp: Nhiễm trùng đường tiết niệu, tăng sản tuyến tiền liệt lành tính (gặp 1% đến 10%). Không phổ biến: Viêm bàng quang , rối loạn cương dương , nấm candida âm hộ (gặp 0,1% đến 1%).
+ Gan: Phổ biến: ALT tăng lớn hơn hoặc bằng 3 lần giới hạn trên của mức bình thường (1% đến 10%). Không phổ biến: AST tăng lớn hơn hoặc bằng 3 lần giới hạn trên của mức bình thường, chức năng gan bất thường (0,1% đến 1%).
+ Hô hấp: Rất phổ biến: Nhiễm trùng đường hô hấp trên (ví dụ viêm xoang, viêm nắp thanh quản, viêm thanh quản, viêm mũi họng, đau vòm họng, viêm họng , viêm họng, viêm mũi, viêm amidan, viêm họng) (15%). Thường gặp: Viêm phế quản, viêm xoang, viêm mũi, ho (gặp 1% đến 10%). Không phổ biến: Viêm amiđan (0,1% đến 1%).
+ Khác: Thường gặp: Mệt mỏi, đau bụng, phù ngoại biên (1% đến 10%).
+ Hệ thần kinh: Thường gặp: Nhức đầu , chóng mặt (1% đến 10%).
+ Tim mạch: Thường gặp: Tăng huyết áp, bệnh động mạch vành (1% đến 10%).
+ Da liễu: Không phổ biến: Mụn trứng cá , rụng tóc , phát ban (0,1% đến 1%).
+ Tiêu hóa: Thường gặp: Buồn nôn, viêm dạ dày ruột , khó tiêu , đau bụng trên , táo bón , nôn , đau vòm họng, viêm miệng , khó chịu ở bụng, bệnh trào ngược dạ dày thực quản (1% đến 10%).
- So sánh thuốc:
Chưa có nghiên cứu trực tiếp nào so sánh baricitinib với tofacitinib. Mặc dù cả hai đều là chất ức chế JAK. Hai loại thuốc này ức chế một loại enzyme chung là JAK1, nhưng mỗi loại lại ức chế một loại enzyme nữa khác nhau, baricitinib (Olumiant) ức thế JAK2 còn tofacinib (Xeljanz) lại ức chế JAK3. Một điều không hoàn toàn rõ ràng nếu những khác biệt này đối với viêm khớp dạng thấp sẽ tạo ra sự khác biệt lớn về hiệu quả.
FDA cho biết không nên kết hợp baricitinib với các thuốc ức chế JAK khác và các thuốc sinh học hoặc thuốc ức chế miễn dịch mạnh như DMARDs như azathioprine và cyclosporine, mặc dù có thể kết hợp với methotrexate và một số DMARD khác.
- Biệt dược, dạng thuốc, liều lượng, cách dùng:
Biệt dược: Olumiant (baricitinib). Thuốc dạng viên nén 2 mg, uống mỗi ngày một viên. Thuốc có thể được uống cùng hoặc không có thức ăn. Các thuốc này có thể được sử dụng như đơn trị liệu hoặc kết hợp với methotrexate hoặc DMARD khác.

- Chỉ định:
Điều trị cho người lớn bị viêm khớp dạng thấp hoạt động mức độ trung bình và nặng, có đáp ứng không đầy đủ với một hoặc nhiều liệu pháp đối kháng chất hoại tử khối u (TNF)
- Điều chỉnh liều ở bệnh nhân có bệnh thận:
+ CrCl 60 đến dưới 90 mL / phút: Không nên điều chỉnh.
+ CrCl dưới 60 mL / phút: Không nên dùng.
- Điều chỉnh liều ở bệnh nhân có bệnh gan:
+ Suy gan nhẹ đến trung bình: Không nên điều chỉnh.
+ Suy gan nặng: Không nên dùng.
Tài liệu tham khảo:
2. http://astera.vn/dieu-tri-viem-khop-dang-thap-tai-phap.
3. https://vi.diphealth.com/670-baricitinib-for-rheumatoid-arthritis-4136413-63
4. https://nhathuoclongchau.com/thuoc-goc/baricitinib
5. https://dalieu.vn/thuoc-uc-che-janus-kinase-trong-da-lieu/
6. https://vi.wikipedia.org/wiki/Janus_kinase_2