Giản đồ Davenport (Davenport Diagram) và rối loạn cân bằng acid - base
PGS.TS. Hà Hoàng Kiệm, BV 103, Học viện Quân y
Giản đồ Davenport có 2 trục:
- Trục hoành là pH (6,9 - 7,7)
- Trục tung là HCO3 (mmol/l).
Các đường cong là PaCO2 (phân áp của CO2 máu động mạch).
Trên giản đồ có một vòng tròn được xác định từ các thông số ở người bình thường: pH = 7,38 - 7,42; PaCO2 = 40 mmHg; HCO3 = 25 mmol/l và Hb = 150g/l.
Từ 2 đường tại điểm pH = 7,38 - 7,42 cắt các đường cong PaCO2 ở 40 mmHg và đường thẳng Hb = 150 g/l tạo thành 6 khu vực rối loạn cân bằng acid - base.
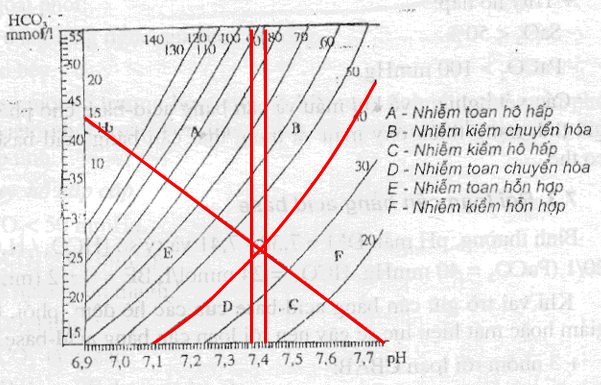
Hình 1. Giản đồ Davenport. Lấy 2 đường tại điểm pH = 7,38 - 7,42 làm mốc thì giản đồ chia 2 phần: Phía trái là nhiễm toan (pH <7,38), trong đó vùng A là nhiễm toan hô hấp (PaCO2 tăng); vùng D là nhiễm toan chuyển hóa (HCO3- giảm); vùng E là nhiễm toan hỗn hợp (PaCO2 tăng và HCO3- giảm). Phía phải là nhiễm kiềm (pH >7,42), trong đó vùng B là nhiễm kiềm chuyển hóa (HCO3- tăng); vùng (C) nhiễm kiềm hô hấp (PaCO2 giảm); vùng F là nhiễm kiềm hỗn hợp (PaCO2 giảm và HCO3- tăng).
1. Nhiễm toan hô hấp (A)
- Rối loạn khởi phát của nhiễm toan hô hấp là tăng PaCO2 do giảm thải CO2 ở phổi. Nguyên nhân:
+ Giảm thông khí phế nang, tắc nghẽn phế quản.
+ Bệnh phổi: phế quản phế viêm, viêm phổi, hen.
+ Hít phải khí CO2, hít lại không khí đã thở.
+ Bị ức chế thần kinh: thuốc ngủ, bại liệt, nhiễm độc, chấn thương sọ não, u não... .
- Xét nghiệm các thông số về cân bằng acd-base cho thấy:
+ pH giảm.
+ PaCO2 tăng.
+ HCO3- máu tăng.
+ CO2 toàn phần máu tăng.
+ Base đệm (BB) giảm, BE âm.
2. Nhiễm kiềm chuyển hóa (B)
- Là trạng thái thừa base hoặc do mất acid không phải là H2CO3.
- Nguyên nhân: là quá dư thừa kiềm do đưa vào cơ thể quá nhiều bicarbonat, hay quá nhiều chất kiềm, hoặc do mất acid trong các trường hợp:
+ Nôn nhiều.
+ Hút dịch dạ dày.
+ ỉa chảy kéo dài.
Kết quả xét nghiệm các thông số cân bằng acid-base:
- pH máu tăng.
- PaCO2 máu tăng.
- CO2 toàn phần máu tăng.
- Bicarbonat (HCO3-) máu tăng.
- Bicarbonat chuẩn (SB) tăng.
- Base đệm (BB) tăng,
- Base dư (BE) dương.
3. Nhiễm kiềm hô hấp (C)
Nhiễm kiềm hô hấp là rối loạn khởi phát do giảm PaCO2; thường gặp trong các trường hợp:
- Tăng thông khí phổi:
+ Giai đoạn đầu của viêm phổi.
+ Sốt cao.
+ Hô hấp nhân tạo quá mức không kiểm tra.
+ Chấn thương sọ não.
- Thở trong khí quyển có phân áp CO2 thấp (khi lên cao).
Khi xét nghiệm các thông số cân bằng acid-base cho thấy:
+ pH máu tăng.
+ HCO3- máu giảm.
+ PaCO2, CO2 toàn phần giảm.
+ BB tăng và BE dương.
4. Nhiễm toan chuyển hóa (D)
- Là trạng thái do mất các anion đệm, chủ yếu là HCO3- hoặc do tích lũy các acid “cố định”, trong thực tế là các acid mạnh mà anion của nó không thể bài xuất qua thận.
- Kết quả xét nghiệm trong nhiễm toan chuyển hóa cho thấy:
+ pH máu giảm mạnh.
+ PaCO2 giảm mạnh.
+ CO2 toàn phần máu giảm.
+ SB giảm, BB giảm.
+ BE âm.
- Nhiễm toan chuyển hóa có thể gặp trong các trường hợp:
+ Đái tháo đường do ứ đọng các thể cetonic.
+ Phù phổi cấp, động kinh, rối loạn chuyển hóa glucid gây ứ đọng acid lactic.
+ Các bệnh thận: viêm thận cấp và mạn không đào thải được acid.
+ ỉa chảy cấp làm mất HCO3-.
Nhiễm toan chuyển hóa có nguy cơ tử vong cao nhất so với các rối loạn cân bằng acid-base khác.
5. Nhiễm toan hỗn hợp (E)
Nhiễm toan hỗn hợp là sự kết hợp nhiễm toan chuyển hóa và nhiễm toan hô hấp.
- Kết quả xét nghiệm trong nhiễm toan hỗn hợp cho thấy:
+ pH máu giảm mạnh.
+ PaCO2 tăng.
+ HCO3- giảm.
+ BE âm.
- Có thể gặp nhiễm toan hỗn hợp trong các trường hợp:
+ Suy hô hấp: phù phổi cấp làm giảm thông khí phế nang, tăng PaCO2, gây thiếu oxy và gây ứ đọng acid lactic.
+ Viêm cầu thận mạn kết hợp với hen phế quản.
+ Phế quản phế viêm.
6. Nhiễm kiềm hỗn hợp (F)
Nhiễm kiềm hỗn hợp là sự kết hợp nhiễm kiềm hô hấp và nhiễm kiềm chuyển hóa.
- Kết quả xét nghiệm cho thấy:
+ pH máu tăng mạnh.
+ PaCO2 giảm.
+ HCO3- tăng.
+ BE dương.
Gặp trong các trường hợp như:
+ Hôn mê gan.
+ Hôn mê do thuốc ngủ sau khi điều trị phối hợp thông khí nhân tạo với kiềm máu để loại trừ thuốc ngủ.
Ảnh hưởng của rối loạn cân bằng acid – base
Chức năng tế bào bình thường đòi hỏi nồng độ của các proton tự do ([H+]) trong chất lỏng cơ thể phải được duy trì trong một giới hạn nhất định, giới hạn này rất hẹp từ 16-160 nM (pH: 6,8-7,8), ngoài giới hạn này thì tế bào sẽ bị tổn thương. Các protein quan trọng như enzyme, chất vận chuyển, kênh ion, hormone peptide, thụ thể và phân tử protein trung gian rất nhạy cảm với sự thay đổi của nồng độ [H+] trong môi trường của chúng. Bán kính nhỏ của H+ (10-9 m hoặc 10-15 mét) cho phép nó tiếp cận và tương tác với các vị trí phản ứng trong phân tử protein, làm thay đổi cấu trúc và chức năng của phân tử protein.
Rối loạn cân bằng nội môi, nhiễm axit là phổ biến, đặc biệt đi kèm với các biến chứng tim mạch, phổi, chuyển hóa và/hoặc bệnh thận cấp tính. Những sai lệch của nồng độ [H+] ngoài phạm vi bình thường có thể có ảnh hưởng sâu sắc đến chuyển hóa tế bào và chức năng màng tế bào. Những sai lệch nghiêm trọng có thể dẫn đến hôn mê và tử vong. Phạm vi nồng độ [H+] tương thích với cuộc sống là khoảng 16-160 nM (pH: 6,8-7,8), thích hợp nhất là pH = 7,38 - 7,42.