PGS.TS. Hà Hoàng Kiệm, BV 103
1. Nguồn gốc và bản chất của corticoid
Corticoid còn gọi là glucocorticoid (cortisol và hydrocortisol) là các hormon của tuyến thượng thận, chúng được tiết ra từ các tế bào lớp bó (zona fasciculata) của vỏ tuyến thượng thận. Đây là hormon vô cùng quan trọng, bắt buộc đối với sự sống và được coi là “hormon stress”. Bình thường tuyến thượng thận tiết lượng hormon steroid với nồng độ cao nhất vào máu vào khoảng 8 giờ sáng, sau đó giảm dần và thấp nhất vào nửa đêm về sáng rồi lại tăng dần. Nồng độ cortisol trong máu lức 8h sáng khoảng 6,6-19,3 mg/l, và 16h vào khoảng 2,3-12,3 mg/l.
Vỏ thượng thận bài tiết corticoid dưới sự điều khiển của trục dưới đồi- tuyến yên-tuyến thượng thận.
Nồng độ cortisol trong máu giảm là yếu tố kích thích vùng dưới đồi thị tiết CRH, đến lượt CRH kích thích tuyến yên bài tiết ACTH, ACTH kích thích vỏ thượng thận phát triển và bài tiết cortisol.
Nồng độ cortisol trong máu tăng là yếu tố ức chế vùng dưới đồi (con đường feedback dài), và tuyến yên (con đường feedback ngắn) làm ngưng tiết CRH và ACTH. Đó là cơ chế feedback nhằm giữ mức hormon trong máu ổn định.
Mỗi ngày cơ thể tiết độ 15-25 mg cortisol, khi có stress lượng này tăng gấp 2-3 lần, thậm chí đến mười lần so với bình thường. Vì vậy, khi ta đưa corticoid vào cơ thể trong thời gian dài theo cách nào đó làm duy trì nồng độ corticoid trong máu trên mức sinh lý sẽ làm ức chế tiết CRH và ACTH gây teo vỏ thượng thận và suy tuyến thượng thận.
Về nhịp bài tiết ngày đêm, cortisol trong máu tăng từ 4 giờ sáng đạt tới mức cao nhất lúc 8 giờ sáng, sau đó giảm dần đến 12 giờ đêm là thấp nhất. Vậy tuyến thượng thận “ngủ” về đêm, nếu ta uống thuốc vào buổi chiều tối tuyến thượng thận bị ức chế suốt ngày và nếu tình trạng ấy kéo dài nhiều ngày sẽ gây suy teo vỏ thượng thận. Vì vậy, khi sử dụng corticoid kéo dài chỉ nên uống vào buổi sáng hoặc dùng thuốc cách ngày.
Công thức hóa học của corticoid là C21H30O5
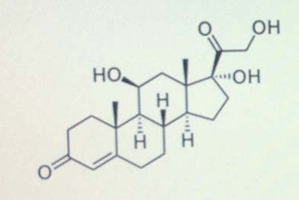
Hình 1. Cấu trúc hóa học của phân tử corticoid
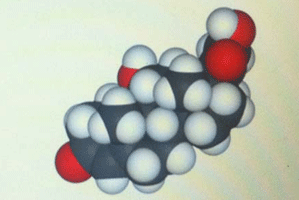
Hình 2. Cấu trúc không gian của phân tử corticoid
2. Vai trò sinh học của corticoid
Corticoid là một hormon có tác dụng cả trên chuyển hóa và trên các mô, các cơ quan của cơ thể.
2.1. Tác dụng trên chuyển hóa
+ Chuyển hóa glucid: corticoid làm tăng tân tạo glucose từ protid và lipid, làm giảm sử dụng glucose ở các mô, làm tăng glucose trong máu và tăng tích lũy glucogen ở gan. Vì thế corticoid có xu hướng làm xuất hiện đái tháo đường hoặc làm nặng thêm bệnh đái tháo đường.
+ Chuyển hóa protid: corticoid làm tăng thoái biến protid, làm giảm vận chuyển acid amin vào trong tế bào, làm tăng nồng độ acid amin trong máu dẫn đến cân bằng nitơ âm và gây teo cơ. Do corticoid làm tăng dị hóa protein nên khi nồng độ corticoid trong máu tăng cao kéo dài, sẽ làm nhiều mô bị ảnh hưởng như mô liên kết kém bền có thể gây ra các vạch rạn dưới da, mô lympho như tuyến ức, lách, hạch bị teo. Xương bị thưa do làm teo mô liên kết của xương, vì mô liên kết của xương vốn là khung để các chất vô cơ như calci, phospho lắng đọng, do đó xương dài và xương dẹt dễ bị gãy, đốt sống dễ bị xẹp lún, có thể gây hoại tử vô khuẩn chỏm xương đùi.
+ Chuyển hóa lipid: corticoid làm tăng phân hủy lipid trong các tế bào mỡ, làm tăng acid béo tự do trong máu. Corticoid làm phân bố lại lipid trong cơ thể, làm tích mỡ ở mặt, cổ, nửa trên thân mình, trong khi các chi bị teo.
+ Chuyển hóa nước và điện giải:
- Na+: corticoid làm tăng tái hấp thu Na+ và nước ở ống thận dễ gây ra phù và tăng huyết áp.
- K+: corticoid làm tăng thải K+ và cả H+ dễ gây nhiễm kiềm máu giảm K+ và nhiễm kiềm giảm Cl-.
- Ca2+: corticoid làm tăng thải Ca2+ qua thận, làm giảm hấp thu Ca2+ ở ruột do đối kháng với vitamin D nên corticoid có khuynh hướng làm giảm Ca2+máu.
- Nước: corticoid có khuynh hướng giữ nước do giữ Na+.
2.2. Tác dụng trên các mô và các cơ quan
+ Hệ thần kinh: corticoid gây kích thích thích hệ thần kinh trung ương, gây hưng phấn lạc quan, có thể cải thiện nhanh triệu chứng bệnh lý. Về sau gây bứt rứt, bồn chồn, lo âu, khó ngủ có thể do rối loạn trao đổi natri, kali trong dịch não tủy. Corticoid gây thèm ăn do tác dụng lên vùng dưới đồi.
+ Mô máu: corticoid làm tăng đông máu, tăng số lượng hồng cầu, bạch cầu, tiểu cầu, nhưng làm giảm số lượng tế lào lympho do hủy các cơ quan lympho.
+ Hệ tiêu hóa: corticoid vừa có tác dụng gián tiếp vừa có tác dụng trực tiếp làm tăng tiết acid dịch vị và pepsin, làm giảm sản xuất muxin, giảm tổng hợp prostaglandin E1 và E2 (chất có vai trò bảo vệ niêm mạc dạ dày). Vì vậy khi corticoid có nồng độ cao kéo dài trong máu có thể gây viêm loét dạ dày.
+ Trên mô liên kết: corticoid ức chế nguyên bào sợi, ức chế phát triển mô hạt, do đó corticoid làm chậm liền sẹo vết thương.
Mọi tác dụng sinh học của corticoid cũng đồng thời là nguồn gốc của các tai biến khi dùng corticoid kéo dài. Với nồng độ sinh lý trong máu, corticoid có tác dụng duy trì cân bằng các quá trình chuyển hóa trong cơ thể cũng như duy trì sự phát triển bình thường của các mô. Khi nồng độ corticoid trong máu giảm kéo dài (bệnh suy tuyến thượng thận) sẽ gây ra một loạt các triệu chứng bệnh lý và có thể dẫn đến tử vong. Khi nồng độ corticoid tăng cao kéo dài trong máu, sẽ gây ra một loạt các bệnh lý ở các cơ quan do tác dụng quá mức của hormon trên các cơ quan đó.
3. Tác dụng dược lý của corticoid
3.1. Ngược dòng lịch sử
Corticoid là một hormon của cơ thể, nhưng đã được sử dụng như một thuốc điều trị. Đối với nghành y tế, corticoid vẫn luôn có mặt trong danh mục thuốc thiết yếu và hầu như bác sĩ điều trị nào cũng đều đã từng kê đơn corticoid không chỉ một lần trong cuộc đời hành nghề của mình.
Ngược lại dòng lịch sử cho thấy: Vào năm 1855, Addison đã chứng minh được vai trò quan trọng của corticoid qua thử nghiệm trên chuột. Ông đã phá hủy vỏ thượng thận của chuột và ghi chép lại những ảnh hưởng nặng nề sau đó như sự suy mòn, hạ huyết áp và chết. Chính vì thế mà người ta đã lấy tên ông để đặt cho bệnh suy tuyến thượng thận (bệnh Addison) với biểu hiện suy mòn, sạm da, hạ huyết áp...
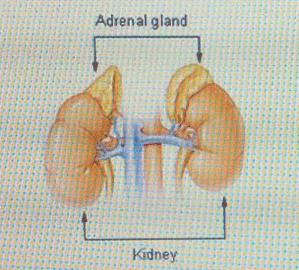

Hình 3: Ảnh tuyến thượng thận (adrenal gland) và nhà bác học Addison.
Người ta bắt đầu ứng dụng chất chiết xuất vỏ thượng thận để điều trị một số trường hợp bệnh nặng nguy kịch, một số bệnh nan y, và thu lượm được những kết quả thật bất ngờ vượt cả mong đợi. Và thế là những mẻ thuốc corticoid đầu tiên được ra đời dưới dạng nguyên thủy nhất, mang sứ mệnh cứu nguời, đó là cortisone. Năm 1949, Hench, Richstein và Kendall đã dùng cortisone để điều trị cho một phụ nữ 29 tuổi gần như tàn phế vì chứng thấp khớp. Thành công này đã mở ra cho những người bệnh thấp khớp một niềm hy vọng lớn vì cho đến thời điểm đó, việc giúp cho người bệnh giảm bớt đau đớn và đưa họ trở về với công việc thường nhật hầu như là điều bất khả kháng. Những đột phá trong điều trị viêm khớp đã đem lại cho êkíp của Hench giải Nobel y học danh giá vào năm sau đó, năm 1950.
Corticoid trở thành một thần dược, các labo tìm cách sản xuất các dạng thuốc có thể tiêm, để có tác dụng nhanh hơn, hoặc thay đổi cấu trúc hóa học để kéo dài thời gian tác dụng của thuốc. Các nhà lâm sàng học thì tìm các ứng dụng điều trị trong nhiều loại bệnh khác nhau từ thấp khớp, cho đến hen suyễn, dị ứng, phù, mề đay, sốc thuốc, các bệnh lý tại các cơ quan khác nhau như thận, da, mạch máu,... có căn nguyên miễn dịch. Trong một số lớn các trường hợp, corticoid cho thấy những khả năng đa dạng của nó và hứa hẹn cho việc giải quyết một số bệnh lý mạn tính.
Tuy nhiên, việc sử dụng ồ ạt và đại trà corticoid cũng làm cho người ta phát hiện ra những tác dụng phụ của thuốc sớm hơn. Sau những ngây ngất vì tác dụng trên cả tuyệt vời của thuốc, người ta lại phải giật mình vì các tác dụng phụ của corticoid. Những gương mặt sưng phù, những thay đổi đáng kể về hình thể như mọc lông mặt, rạn da, gù lưng, những vết thương nhiễm trùng nặng nề, gãy xương, những cơn bột phát của một số bệnh đi kèm... đã làm cho giới chức ngành y phải đưa ra những cảnh báo khẩn cấp cho việc sử dụng corticoid.
Các nhà bào chế và các nhà điều trị học lại bắt đầu lao vào một cuộc tìm kiếm mới, nhằm tận dụng hiệu quả và giảm thiểu hết mức các tác dụng có hại của thuốc. Phương pháp tiêm tại chỗ corticoid ra đời vào thời điểm những năm 1950, gián tiếp thực hiện việc "xét lại" trong quan điểm của ngành y. Việc tập trung liều tấn công tại một vị trí xác định bằng đường dùng toàn thân (uống hay tiêm mạch) đòi hỏi phải sử dụng corticoid với liều lượng khá cao, và điều này cũng kéo theo tăng nguy cơ bị các tác dụng phụ của thuốc. Mục tiêu của liệu pháp corticoid tại chỗ là tập trung tại vị trí bệnh một liều điều trị đủ để đánh gục quá trình viêm đang ngoan cố mà không gây tác hại đến môi trường chung là các cơ quan khác trong cơ thể.
Bên cạnh những ích lợi đáng kể của liệu pháp corticoid tại chỗ, một lần nữa người ta lại phải có những cảnh báo về những tác dụng không mong muốn của nó để các bác sĩ và bệnh nhân lưu ý.
3.2. Tác dụng điều trị của corticoid
Corticoid có 3 tác dụng chính là chống viêm, chống dị ứng và ức chế miễn dịch. Tuy nhiên những tác dụng này chỉ đạt được khi nồng độ corticoid trong máu cao hơn nồng độ sinh lý, nhưng đó cũng là nguyên nhân dẫn đến các tác dụng không mong muốn. Vì vậy, trong trường hợp có thể nên dùng thuốc tại chỗ hơn là dùng đường toàn thân, nếu phải dùng đường toàn thân thì nên dùng liều thấp nhất có tác dụng.
3.2.1. Tác dụng ngăn cản phản ứng viêm
Corticoid có tác dụng ức chế phản ứng viêm của cơ thể, nó tác dụng trên nhiều giai đoạn khác nhau của quá trình viêm, không phụ thuộc vào nguyên nhân gây viêm.
+ Ức chế mạnh sự di chuyển của bạch cầu về ổ viêm.
+ Làm giảm sản xuất và giảm hoạt tính nhiều chất trung gian hóa học của viêm như histamin, serotonin, bradykinin, các dẫn xuất của acid arachidonic (các prostaglandin). Tác dụng này là gián tiếp vì corticoid làm tăng sản xuất lipocortin, là một protein có trong tế bào có tác dụng ức chế phospholipase A2. Khi phospholipase A2 bị ức chế làm phospholipid không chuyển thành acid arachidonic được.
+ Ức chế giải phóng men tiêu thể và các gốc tự do superoxyd, làm giảm hoạt tính của các yếu tố hóa ứng động, giảm hoạt tính các chất hoạt hóa plasminogen, collagenase, elastase…
+ Làm giảm hoạt động thực bào, giảm chỉ số thực bào của các đại thực bào, các bạch cầu đa nhân, giảm sản xuất các cytokin.
3.2.2. Tác dụng chống dị ứng
Phản ứng dị ứng của cơ thể xảy ra do các IgE hoạt hóa gắn lên các receptor đặc hiệu của tế bào mastocyte và bạch cầu ái toan dưới tác dụng của dị nguyên. Sự gắn kết này gây hoạt hóa phospholipase C. Enzym này được hoạt hóa sẽ làm tách phosphatidyl-inositol diphosphat ở màng tế bào thành diacyl-glycerol và inositoltriphosphat. Hai chất này đóng vai trò “người truyền tin thứ hai” làm các hạt ở bào tương tế bào mastocyte giải phóng các chất trung gian hóa học của phản ứng dị ứng như histamin, serotonin… và gây ra dị ứng.
Bằng cách ức chế phospholipase C, coticoid đã phong tỏa giải phóng chất trung gian hóa học gây phản ứng dị ứng. Như vậy IgE gắn trên tế bào mastocyte, nhưng không hoạt hóa được tế bào mastocyte. Corticoid là chất chống dị ứng mạnh.
3.2.3. Tác dụng ức chế miễn dịch
Corticoid có tác dụng chủ yếu trên miễn dịch tế bào, ít ảnh hưởng đến miễn dịch dịch thể. Tác dụng của corticoid trên miễn dịch biểu hiện ở nhiều khâu:
+ Ức chế tăng sinh tế bào lympho T do làm giảm sản xuất interleukin-1 từ đại thực bào và interleukin-2 từ tế bào lympho T4.
+ Giảm hoạt tính gây độc tế bào của các lympho T (T8) và các tế bào giết tự nhiên NK (natural killer) do ức chế sản xuất interleukin-2 và interferon gamma.
+ Ức chế sản xuất yếu tố hoại tử khối u TNF (tissue necrosese factor) và cả interferon, vì vậy corticoid làm giảm hoạt tính diệt khuẩn, gây độc tế bào và nhận dạng kháng nguyên của đại thực bào.
Các tác dụng ức chế miễn dịch đồng thời cũng là tác dụng chống viêm, đồng thời do ức chế tăng sinh tế bào lympho nên corticoid có tác dụng tốt trong điều trị bệnh bạch cầu lympho cấp, bệnh Hodgkin.
4. Các chế phẩm corticoid
4.1. Chế phẩm
Mọi corticoid dùng trong điều trị đều là dẫn xuất của cortisol hay hydrocortison (hormon tự nhiên có OH ở vị trí 11). Bằng cách thay đổi cấu trúc của cortisol, người ta có thể làm tăng mạnh tác dụng chống viêm và thời gian bán thải trừ của thuốc, đồng thời làm giảm khả năng giữ muối và nước.
+ Vòng A: khi có thêm đường nối kép giữa vị trí 1 - 2, tác dụng chống viêm tăng và giữ muối giảm (prednison, prednisolon).
+ Vòng B: thêm -CH3 ở vị trí 6 alpha (methylprednisolon), hoặc Flo (F) ở vị trí 9 alpha, hoặc ở cả 2 vị trí 9 - 6 alpha (fludrocortison, flucinonid), tác dụng chống viêm càng mạnh và kéo dài thời gian bán thải (t ½). Nhưng F ở vị trí 9 alpha lại làm tăng tác dụng giữ Na+.
+ Vòng D: thêm -CH3 hay -OH ở vị trí 16 alpha, làm giảm mạnh khả năng giữ muối của hợp chất 9 alpha F (triamcinolon, dexametason, betametason).
Vì thế hiện nay có rất nhiều chế phẩm corticoid mạnh và tác dụng dài. Liều lượng và thời gian dùng rất khác nhau, khi sử dụng cần lưu ý để tránh tai biến cho bệnh nhân. Theo thời gian tác dụng hiện nay người ta có 3 loại sau:
- Thời gian tác dụng ngắn : t1/2 =8 –12 giờ.
- Thời gian tác dụng trung bình: t1/2 = 12 –36 giờ.
- Thời gian tác dụng dài: t1/2 = 36 – 72 giờ.
Bảng 1. Một số corticoid thường dùng
Tên thuốc - TDchống viêm - TD giữ Na - Chuyển hóa đường - T1/2 sinh học - Liều tương đương
Thuốc tác dụng ngắn (12h)
Cortison 0,8 0,8 0,8 8-12h 25mg
Hydrocortison 1 1 1 8-12h 20mg
Thuốc TD trung bình (12-36h)
Prednison 4 0,8 4 12-36h 5mg
Prednisolon 4 0,8 4 12-36h 5mg
Methylprednisolon 5 0,5 5 12-36h 4mg
Triamcinolon 5 0 5 12-36h 4mg
Thuốc TD dài (36-54h)
Betametason 25-30 0 25 36-54h 0,75mg
Dexammetason 25-30 0 25 36-54h 0,75mg
Nhìn vào bảng trên chúng ta thấy rằng nếu dùng methylprednisolon với cùng liều lượng và thời gian tương đương prednisolon thì biến chứng tiểu đường sẽ gặp nhiều hơn, nhưng ít giữ natri hơn.
4.2. Dược động học
Corticoid được hấp thu dễ dàng qua đường tiêu hóa, t1/2 huyết tương khoảng từ 90- 300 phút. Trong huyết tương, cortisol gắn với transcortin (90%) và với albumin (6%). Cortisol bị chuyển hóa chủ yếu ở gan bằng khử đường nối 4 - 5 và khử ceton ở vị trí 3. Thải trừ qua thận dưới dạng sulfo- và glycuro-liên hợp.
Một số chế phẩm dạng tiêm có tá dược là polyetylen glycol, glysorbat... làm thuốc thải trừ rất chậm, tuỳ theo bệnh và liều lượng, có thể chỉ tiêm 1 tuần, 2 tuần hoặc 1 tháng 1 lần, như Depomedrol (chứa metylprednisolon acetat 40 mg trong 1 ml), Rotexmedica, Kenacort (chứa triamcinolon acetonid 40 - 80 mg/ml). Tuy nhiên, loại này thường có nhiều tác dụng phụ như teo da, teo cơ, xốp xương và rối loạn nội tiết.
5. Các chỉ định và chống chỉ định điều trị chính
5.1. Chỉ định
+ Chỉ định bắt buộc khi cần thay thế sự thiếu hụt hormon:
- Suy thượng thận cấp
- Suy thượng thận mạn tính (bệnh Addison)
+ Chỉ định thông thường trong chống viêm và ức chế miễn dịch
- Viêm khớp, viêm khớp dạng thấp
- Bệnh thấp tim
- Bệnh thận: Hội chứng thận hư
- Các bệnh collagen (collagenose): Lupus ban đỏ, xơ cứng bì (sclerodermia), viêm đa cơ, viêm quanh động mạch dạng nút, viêm đau nhiều cơ do thấp
- Bệnh dị ứng
- Hen phế quản
- Bệnh ngoài da
- Bệnh ung thư: Phối hợp với thuốc gây độc tế bào để trị các bệnh ác tính: bệnh Hodgkin, bệnh bạch cầu lympho cấp. Điều trị phù não ở bệnh nhân bị di căn, hoặc bị khối u não nguyên phát (dùng dexamethason), là thành phần trị nôn do hóa trị liệu ung thư.
- Chống thải ghép cơ quan: ghép thận, ghép gan, ghép tim…
5.2. Chống chỉ định
+ Mọi nhiễm khuẩn hoặc nấm chưa có điều trị đặc hiệu
+ Viêm, loét dạ dày- hành tá tràng
+ Loãng xương
+ Nhiễm virus viêm gan
+ Chỉ định thận trọng trong đái tháo đường, tăng huyết áp.
5.3. Những điểm cần chú ý khi dùng thuốc
+ Khi dùng corticoid tự nhiên (cortisol, hydrocortison) phải ăn nhạt. Đối với thuốc tổng hợp, ăn tương đối nhạt.
+ Luôn cho một liều duy nhất vào 8 giờ sáng sau ăn để hạn chế tác dụng phụ gây suy tuyến thượng thận.
+ Dùng liều tối thiểu có tác dụng
+ Kiểm tra định kỳ nước tiểu, huyết áp, glucose máu, dạ dày, xương cột sống, kali máu, thăm dò chức phận trục hạ khâu não- tuyến yên- thượng thận.
+ Dùng thuốc phối hợp: tăng liều insulin đối với bệnh nhân đái tháo đường, phối hợp kháng sinh nếu có nhiễm khuẩn.
+ Chế độ ăn: nhiều protein, calci và kali, ít muối, đường và lipid. Nếu phải dùng corticoid kéo dài, có thể dùng thêm vitamin D như Dedrogyl 5 giọt/ ngày (mỗi giọt chứa 0,005mg 25 - OH vitamin D3), decadurabolin dạng tiêm, mỗi tuần tiêm bắp 1 ống để tăng quá trình đồng hóa đạm.
+ Tuyệt đối vô khuẩn khi dùng corticoid tiêm vào ổ khớp
Sau một đợt dùng kéo dài (trên hai tuần) với liều cao khi ngừng thuốc đột ngột bệnh nhân có thể tử vong do suy thượng thận cấp, biểu hiện các triệu chứng tiêu hóa, mất nước, giảm Na+, giảm K+ máu, suy nhược, ngủ lịm, tụt huyết áp. Vì thế không được ngừng thuốc đột ngột.
6. Tác dụng không mong muốn có thể gặp
6.1. Với hệ cơ xương
+ Đau cơ, teo cơ, yếu cơ do tác dụng dị hóa protein của corticoid
+ Loãng xương, có thể gây gãy xương tự phát hoặc sau một sang chấn nhẹ, xẹp lún thân đốt sống, hoại tử vô khuẩn chỏm xương đùi. Làm chậm liền xương ở bệnh nhân gãy xương.
6.2. Với hệ tiêu hóa
+ Gây viêm hoặc loét dạ dày, tá tràng
+ Chảy máu dạ dày, tá tràng, có thể xảy ra trên bệnh nhân đã có viêm hoặc loét dạ dày, tá tràng từ trước, nhưng cũng có thể xảy ra ở bệnh nhân không có viêm loét dạ dày tá tràng trước đó.
+ Thủng dạ dày
+ Thủng ruột
+ Viêm tụy
6.3. Với hệ tim mạch
+ Huyết áp tăng cao hơn đòi hỏi phải tăng liều thuốc hạ huyết áp đối với bệnh nhân đã có tăng huyết áp, hoặc xuất hiện tăng huyết áp sau khi dùng thuốc ở bệnh nhân trước đó chưa có tăng huyết áp.
+ Làm suy tim ứ huyết nặng lên do giữ muối, giữ nước.
+ Gây kiềm máu dẫn tới giảm kali máu nặng khi kết hợp với thuốc lợi tiểu thải muối.
6.4. Với chuyển hóa
+ Làm khởi phát đái tháo đường hoặc làm đái tháo đường nặng lên
+ Có thể gây hôn mê do tăng thẩm thấu ở bệnh nhân đái tháo đường
+ Gây tăng mỡ máu
+ Gây hội chứng Curshing
6.5. Với hệ nội tiết
+ Làm trẻ em chậm lớn, suy dinh dưỡng
+ Gây vô kinh thứ phát ở phụ nữ
+ Mất điều chỉnh hệ dưới đồi-tuyến yên-tuyến thượng thận, có thể xảy ra suy chức năng tuyến thượng thận cấp nếu ngừng thuốc đột ngột hoặc suy thượng thận mạn.
6.6. Với hệ thần kinh
+ Gây rối loạn tâm thần
+ Giảm hoạt động điện não
6.7. Với mắt
+ Gây tăng nhãn áp (glocom)
+ Đục thủy tinh thể sau và dưới bao
6.8. Ức chế sự tăng sinh và phát triển của tế bào xơ
+ Làm chậm liền sẹo vết thương
+ Teo tổ chức dưới da
6.9. Gây giảm đáp ứng miễn dịch
+ Bệnh nhân dễ bị nhiễm khuẩn
+ Làm bùng phát bệnh lao, viêm gan virus
6.10. Hội chứng sau cắt thuốc
+ Suy thượng thận cấp do ngừng thuốc đột ngột, có thể tử vong
+ Suy thượng thận muộn
Nếu dùng corticoid để chống viêm và ức chế miễn dịch thì tất cả tác dụng chuyển hóa của corticoid là các tác dụng không mong muốn.
7. Biểu hiện lâm sàng một số biến chứng
7.1. Suy tuyến thượng thận cấp
Suy thượng thận cấp có thể xảy ra khi dùng liều cao trên 2 tuần hoặc dùng liều thấp nhưng kéo dài nhiều tháng mà ngừng đột ngột, tuyến thượng thận đang bị ức chế không tiết corticoid, làm nồng độ corticoid trong máu giảm đột ngột. Vì vậy khi dùng corticoid liều cao trên 2 tuần hoặc dùng liều thấp nhưng thời gian kéo dài, trước khi ngừng thuốc bắt buộc phải giảm liều từ từ.
+ Biểu hiện lâm sàng: mất nước, kèm rối loạn chuyển hóa như tăng K+ huyết, nhiễm acid, giảm đường huyết, ngủ gà, vô lực, tụt huyết áp, trụy tim mạch, tử vong.
+ Xử trí cấp cứu:
- Lập tức dùng corticoid liều cao như hydrocortison hemisuccinat 100mg tiêm tĩnh mạch mỗi 6 giờ.
- Phối hợp truyền nước muối sinh lý và glucose để hồi phục thể tích tuần hoàn. Nếu cung cấp đủ nước và chất điện giải thì không cần thêm mineralocorticoid.
- Nếu đã kiểm soát được tình trạng cấp thì giảm liều corticoid tiêm tĩnh mạch để chuyển sang điều trị duy trì bằng đường uống.
- Nếu các bệnh nhân này phải trải qua giải phẫu thì trước phẫu thuật 1 ngày phải uống 2 - 3 lần liều bình thường. Vào ngày phẫu thuật cho hydrocortison 50 – 100 mg mỗi 4 – 6 giờ, nhớ theo dõi lượng dịch và chất điện giải cẩn thận.
- Khi bệnh nhân đã hồi phục thì giảm từ liều cao về liều uống trong vài ngày.
7.2. Suy tuyến thượng thận mạn
Nếu dùng kéo dài corticoid, tuyến thượng thận có thể bị teo và giảm hoặc mất chức năng gây ra suy thượng thận mạn. Nên nhớ cần 2-3 tháng để tuyến yên đáp ứng trở lại và 6-9 tháng, thậm chí 1 năm sau nồng độ cortisol mới trở về mức bình thường. Người ta thường tiêm bắp synacthen (ACTH) ống 1mg, một tuần 1-2 ống, tổng số khoảng 3-4 ống để kích thích phục hồi chức năng tuyến thượng thận sau khi ngừng corticoid.
+ Biểu hiện lâm sàng giống như bệnh Addison (suy chức năng tuyến thượng thận nguyên phát) nhưng mức độ triệu chứng nhẹ hơn, có 4 triệu chứng chính:
- Da xạm đen: giống màu chì, da thường thâm ở các vùng:
. Lúc bình thường da đã thâm (như đầu vú, bẹn)
. Chỗ da không được che kín
. Nơi da thường bị cọ xát (cùi tay, đầu gối, vai, nơi cọ xát, dải rút và thắt lưng)
. Niêm mạc cũng bị xám đen (niêm mạc môi, lưỡi)
- Mệt nhọc: cơ lực giảm đi nhanh chóng. Dùng lực kế để thử cơ lực người bệnh bóp lần đầu, sức bóp có thể bình thường, các lần bóp kế tiếp, sức bóp giảm đi nhanh. Khi làm việc, người bệnh chóng bị mệt mỏi, sự mệt mỏi tăng lên trong đợt tiến triển.
- Huyết áp hạ: hạ cả số huyết áp tâm thu và huyết áp tâm trương, nhất là trong đợt tiến triển. Người bệnh bị nhức đầu hoa mắt, có xu hướng thỉu đi.
- Gầy, xút nhanh: trong vài tháng có thể xút 3–4 kg
+ Điều trị: phải điều trị thay thế bằng dùng corticoid thường xuyên
7.3. Hội chứng Curshing
Hội chứng Curshing xảy ra khi dùng corticoid liều cao trên 1 tháng hoặc liều thấp nhưng kéo dài. Biểu hiện của hội chứng curshing nguyên phát (cường chức năng vỏ thượng thận) hoặc thứ phát đều giống nhau về mặt lâm sàng.
+ Triệu chứng lâm sàng: nổi bật nhất là sự biến dạng của người bệnh, người bệnh trở nên béo một cách đặc biệt.
- Mặt béo tròn, húp cả mắt, má phình, cằm đôi, cổ cũng béo tròn. Thân cũng béo, bụng to phệ, vú to, lưng có từng cục mỡ.
- Trái lại các chi trên và chi dưới nhỏ đi, gầy khẳng khiu.
- Da mặt đỏ hồng, hơi tím ở má, nhưng đặc biệt là các nếp nhăn dài, đỏ thẫm hơn da bình thường, các nếp nhăn dài này thường thấy ở bụng dưới, lưng, vú.
- Xuất hiện những nếp rạn da ở hai bên đùi gần bẹn vùng dưới vú, vùng da bụng.
- Lông mọc nhiều, ngay cả nơi không có nay cũng thấy như: đàn bà mọc râu mép như đàn ông.
- Nhiều mụn trứng cá ở mặt, nửa trên lưng.
- Huyết áp tăng cao: huyết áp tâm thu có thể tới 150-200 mmHg, huyết áp tâm trương từ 100-140 mmHg.
- Mệt nhọc, làm người bệnh không muốn vận động.
- Rối loạn tình dục: đàn ông có thể liệt dương, đàn bà mất kinh.
+ Điều trị: điều trị triệu chứng, nếu tăng huyết áp điều trị hạ huyết áp, dùng các thuốc tăng đồng hóa đạm, hạ lipid máu… sau khi ngừng corticoid các triệu chứng của hội chứng curshing sẽ giảm dần.
7.4. Chậm phát triển ở trẻ em
+ Sử dụng corticoid liều cao trong thời gian dài sẽ làm chậm phát triển chiều cao của trẻ em do corticoid ức chế tác dụng làm phát triển xương và sụn của somatomadin C (somatomadin C là tác nhân gây phân bào do gan, nguyên bào sợi và mô ngoại biên bài tiết).
+ Để giảm hậu quả của tác dụng này nên hạn chế việc kê đơn corticoid cho trẻ em. Nếu phải dùng thì dùng liều thấp có hiệu quả và trong thời gian ngắn nhất. Khi phải dùng kéo dài thì dùng phương pháp điều trị liều cao cách ngày thay cho cách dùng hằng ngày để giảm ức chế tuyến thượng thận, tuyến sinh dục và tuyến giáp. Khuyến khích trẻ em chơi thể dục, thể thao, ăn nhiều chất đạm và calci. Bổ xung thêm các chất tăng đồng hóa đạm như durabolin, các vitamin.
7.5. Loãng xương
+ Ở liều sinh lý corticoid có tác dụng tích cực trên chuyển hóa calci và xương, nhưng ở liều điều trị và dùng kéo dài sẽ gây mất xương. Có đến 30-50% bệnh nhân bị gãy xương không có chấn thương khi sử dụng corticoid liều cao và kéo dài, do corticoid làm tăng tiêu xương (tăng chức năng hủy cốt bào và làm tiêu tổ chức liên kết trong xương). Tác dụng trên xương của corticoid là tác dụng phức tạp và có liên quan đến liều dùng. Tác dụng tăng chức năng hủy cốt bào là gián tiếp thông qua sự tăng bài tiết PTH được kích thích bởi sự giảm calci huyết. Tác dụng mất xương còn được tăng cường do corticoid làm giảm mức Ca2+ huyết thông qua cơ chế làm giảm hấp thu calci ở ruột và tăng bài xuất calci qua nước tiểu. Sự mất xương nhanh nhất là ở 6-12 tháng đầu sử dụng corticoid và trở về mức như người không dùng thuốc trong 1-2 năm. Sự mất xương thường dẫn đến gãy xương đối với bệnh nhân có tỉ trọng xương thấp vào thời điểm khởi đầu dùng corticoid. Người già và phụ nữ sau mãn kinh có nguy cơ gãy xương cao. Tất cả xương đều bị ảnh hưởng, đặc biệt là xương sườn và xương sống. Liều prednison 7,5mg/ngày có khả năng gây mất xương cho tất cả các bệnh nhân, nam và nữ bị ảnh hưởng như nhau.
Đường xông hít (inhale) trong thời gian dài có lẽ gây mất xương tối thiểu, trừ khi dùng liều lớn. Hoại tử xương không do nhiễm khuẩn và teo cơ là các tác dụng phụ nguy hiểm nhất do corticoid. Thường xảy ra ở đầu xương cánh tay hay đầu xương đùi, gây đau dữ dội và giảm cử động.
+ Dự phòng và điều trị: Để giảm thiểu tai biến gãy xương do corticoid nên giảm liều đến mức thấp nhất nếu có thể và giảm thời gian sử dụng thuốc. Sử dụng thuốc cách ngày dường như không làm giảm sự mất xương.
Thay đổi nếp sống, bỏ thuốc lá, tránh uống nhiều rượu, không khiêng vác nặng, tập thể dục đều đặn (30-60phút/ngày).
Bổ sung calci trong thời gian dùng thuốc 1000 mg/ngày, vitamin D 400 đơn vị/ngày. Điều trị thay thế estrogen cho phụ nữ sau mãn kinh nếu không có chống chỉ định. Trong trường hợp loãng xương có thể điều trị bằng Calcitonin và bisphosphat.
Nên theo dõi tỉ trọng xương cho tất cả các bệnh nhân sau 6 tháng sử dụng corticoid.