Các virus viêm gan
Cho tới nay ít nhất đã có 6 loại virus viêm gan được ghi nhận và kí hiệu là:
- HAV (Hepatitis A virus): virus viêm gan A
- HBV (Hepatitis B virus): virus viêm gan B
- HCV (Hepatitis C virus): virus viêm gan C
- HDV (Hepatitis D virus): virus viêm gan D (còn gọi là virus delta)
- HEV(Hepatitis E virus): virus viêm gan E
- HGV (Hepatitis G virus): virus viêm gan G
Ngoài ra, một vài virus viêm gan khác còn đang tiếp tục nghiên cứu. Trong các loại virus viêm gan kể trên, vai trò gây bệnh của HGV còn chưa thật rõ.
Một loại virus có gây tổn thương gan nhưng không được xếp vào nhóm các virus viêm gan (các virus hường gan) cần được kể đến là:
- CMV (Cytomegallovirus)
- EBV (Epstein Barr Virus)
- HSV (Herpes simplex virus)
- Virus Dengue, virus Marburg, virus Ebola, virus Lassa…
Tuy nhiên, việc nghiên cứu tìm các loại virus gây viêm gan mới đang còn tiếp tục. Người ta nhận thấy rằng ngoài các virus kể trên, vẫn có thể còn các virus gây viêm gan khác chưa được xác định. Gần đây, virus gây bệnh viêm gan sau truyền máu (TTV – Transfusion Transmitted virus) đã được phát hiện và ghi nhận.
Các virus viêm gan và đường lây:
|
|
HAV |
HBV |
HCV |
HDV |
HEV |
HGV |
|
Họ virus |
Picornaviri-dae |
Hepadna-viridae |
Flavivi-ridae |
|
Calcivir-dae |
Flavi-viridae |
|
Hình thể |
H. khối |
H. cầu |
H. khối |
H. cầu |
H. khối |
? |
|
Vỏ bọc |
Không |
Có |
Có |
Có |
Không |
Có |
|
Đường kính (mm) |
27 – 28 |
42 – 45 |
60 – 80 |
35 – 37 |
32 – 34 |
? |
|
Hệ gen |
ARN dây xoắn đơn, cực tính dương |
AND, 1 phần dây xoắn kép |
ARN dây xoắn đơn, cực tính dương |
ARN dây xoắn đơn, cực tính âm |
ARN dây xoắn đơn, cực tính dương |
ARN, dây xoắn đơn, cực tính dương |
|
Kháng nguyên |
HAV |
HbsAg HbeAg HbcAg |
HCV |
HDV |
HEV |
HGV |
|
Kháng thể |
Anti - HAV |
Anti – HBs Anti – Hbe Anti - HBc |
Anti - HCV |
Anti - HDV |
Anti - HEV |
anti – HGV
|
|
Đường lây nhiễm |
Tiêu hóa |
Đường máu |
Đường máu |
Đường máu |
Tiêu hóa |
Đường máu |
Cần lưu ý rằng bệnh nhân viêm gan virus có thể chỉ do 1 loại virus viêm gan hoặc do đồng nhiễm ≥ 2 loại virus khác nhau gây ra. Người ta đã ghi nhận được các trường hợp đồng nhiễm 2 loại virus (HBV – HDV, HBV – HCV, HBV – HEV), thậm chí 3 loại virus (HBV – HCV – HDV, HBV – HDV – HEV), trong đó đồng nhiễm HBV – HDV thường gặp hơn trong thể bệnh viêm gan kịch phát.
Các virus viêm gan lây truyền theo đường máu có thể có nhiều phương thức lây truyền khác: lây từ mẹ sang con, lây do quan hệ tình dục, lây do truyền máu và các sản phẩm của máu, qua ghép tổ chức, qua dụng cụ y tế…
1. Virus viêm gan A (HAV)
1.1. Cấu trúc
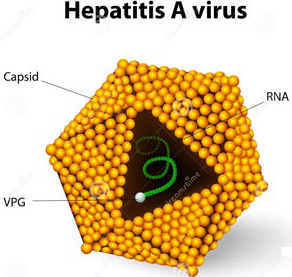
HAV do Feinstone phát hiện ra năm 1973, thuộc họ Picornaviridae. Virus có kích thước rất nhỏ, hình khối đa diện (hoặc hình cầu) đường kính khoảng 28nm. Hệ gen gồm có 1 dây axit ribonucleic (ARN), xoắn dài khoảng 7500 base. Dây này được bao quanh bởi 1 capsid gồm có 3 protein cấu trúc (VP1, VP2 và VP3). HAV không có vỏ bao ngoài.
1.2. Sức đề kháng
HAV là virus có sức chịu đựng cao ở ngoại cảnh và với hóa chất, sống được trong môi trường pH = 3 hay thấp hơn trong 1 giờ, ở nhiệt độ 60 độ C trong 1 giờ. Để lạnh – 20 độ C đến - 70 độ C virus sống được hàng năm và không mất hoạt tính gây bệnh. Virus chỉ bị bất hoạt hoàn toàn bằng Chloramin ở nồng độ 1 mg/lít/30 phút hay ở nhiệt độ 100 độ C trong 30 phút.
1.3. Khả năng gây bệnh
Phần lớn các trường hợp nhiễm HAV không có triệu chứng lâm sàng. Bệnh viêm gan A thường diễn biến lành tính, khỏi hoàn toàn, không chuyển thành mạn tính, không có tình trạng người lành màng virus.
Thể viêm gan tối cấp do HAV rất ít, tỷ lệ tử vong do viêm gan A nặng khoảng 1/1000 – 1/10.000 người bệnh.
1.4. Đáp ứng miễn dịch
Cơ thể sinh kháng thể Anti – HAV. Kháng thể Anti – HAV týp IgM có ngay trong giai đoạn khởi phát và toàn phát của bệnh hiệu giá kháng thể cao nhất ở huyết thanh 1 – 3 tháng, giảm dần và sau 6 – 12 tháng. Kháng thể Anti – HAV týp IgG tồn tại kéo dài nhiều năm. Tuy nhiên có thể vẫn bị tái nhiễm HAV, gây viêm gan A tái nhiễm.
2. Virus viêm gan B (HBV)
2.1. Hình thể và cấu trúc
HBV thuộc họ hepadnavirus là những virus có kích thước nhỏ. Đây là virus viêm gan duy nhất có axit nhân là AND (các virus viêm gan khác đều là ARN).
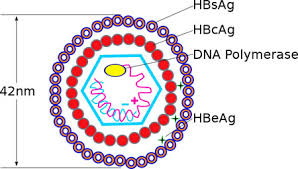
Dưới kính hiển vi điện tử người ta thấy có 3 loại tiểu thể khác nhau:
- Tiểu thể hình cầu nhỏ có đường kính 22nm.
- Tiểu thể hình ống (hình que) có đường kính 20 – 22nm và dài từ 40 – 400nm.
- Tiểu thể hình cầu lớn có đường kính 42 – 45nm còn gọi là tiểu thể Dane, đây chính là virus hoàn chỉnh.
Tiểu thể hình cầu nhỏ và hình ống là thành phần vỏ của HBV mà trong quá trình nhân lên tổng hợp dư thừa. Đây chính là kháng nguyên bề mặt (HbsAg). Các tiểu thể hình cầu nhỏ và hình ống có thể đứng riêng rẽ hoặc đứng với nhau thành từng đám, chúng không có khả năng lây truyền bệnh.
Bộ gen (Genome) của HBV là một phân tử AND vòng có cấu trúc mạch kép không hoàn toàn, kích thước 3200 Base, nó được cấu tạo bởi 2 sợi có chiều dài không bằng nhau. Chuỗi dài nằm ngoài có cực tính âm, tạo nên một vòng tròn liên tục có chiều dài cố định 3,2Kb và mã hóa cho các thông tin di truyền của virus. Chuỗi nằm trong, có cực tính dương thay đổi và chỉ bằng 50 – 80% chiều dài sợi âm. HBV có cấu trúc đặc biệt nhỏ gọn, có được sự liên kết trong cấu trục bộ gen bằng cách sắp xếp những miền giao của các gen: S, C, P và X cho nên có khả năng tổng hợp được nhiều loại Protein quan trọng của virus.
- Gen S: Bao gồm vùng S, Pre – S1 và Pre – S2 mã hóa để tổng hợp các protein bề mặt hay HbsAg. Vùng S, Pre-S2 có chiều dài cố định trong khi đó vùng Pre – S1 có chiều dài thay đổi tùy theo từng phân týp khác nhau.
+ Đoạn gen S tổng hợp nên Protein S (Small) có chiều dài 24 Kd gồm 226 amin (aa). Đây là Protein “chủ yếu” (major) vì nó chiếm đa số. Ở vùng S có ít nhất 5 quyết định kháng nguyên (antigenic determinant) HbsAg. Tùy theo sự phân bố của các quyết định kháng nguyên này mà tạo ra các phân týp khác nhau. Mỗi phân týp đều có chung phần quyết định kháng nguyên “d” hoặc “y” ghép với “w” hoặc “r”. Ngoài ra quyết định kháng nguyên r lại có thêm quyết định phụ r1, quyết định kháng w lại có thêm quyết định phụ w1, w2, w3, w4. Gần đây người ta lại tìm thêm được các quyết định kháng nguyên bổ sung khác như q, x, g.
+ Đoạn gen S và Pre S2 tổng hợp nên Protein M (Medium) có chiều dài 33 Kd gồm 281 aa. Vùng Pre – S2 có vai trò giúp cho virus bám dính và xâm nhập vào trong tế bào gan nhờ nó liên kết với một loại albumin được trùng hợp trong huyết thanh người (pHSA polymerized Human Serum Albumin).
+ Đoạn S, Pre – S1 và Pre – S2 tổng hợp nên Protein L (Large) có chiều dài 39 Kd. Chuỗi Protein Pre – S1 có chiều dài thay đổi theo từng phân týp khác nhau.
- Gen C: Mã hoá các Protein của nucleocapsid. Gen C có hai đoạn: đoạn nhân và đoạn trước nhân.
Nếu sự sao chép từ đoạn trước nhân, sản phẩm Protein và HBeAg. Đây là một loại Protein không tham dự vào cấu trúc của virion và chức năng của nó chưa được biết rõ. Tuy nhiên sự hiện diện của HBeAg có liên quan đến tính lây nhiễm và phản ánh tình trạng đang nhân lên của virus.
Nếu việc sao chép bắt đầu từ vùng nhân, thì sản phẩm protein là HBcAg, nó không có petit tín hiệu nên không được bài tiết ra khỏi tế bào gan, nhưng nó tập trung trong các thể nucleocapsid gắn với RNA và có chức DNA của HBV.
Một số trường hợp xảy ra đột biến ở đoạn Pre-C nên sự tổng hợp HBeAg không thực hiện được mặc dù quá trình nhân đôi của virus vẫn tiếp diễn.
- Gen P: Là gen lớn nhất, chiếm 80% chiều dài của bộ gen, mã hóa cho DNA – Polymerase, enzym có cả hai loại hoạt tính của DNA – Polymerase phụ thuộc DNA và men sao chép ngược phụ thuộc RNA.
- Gen X: Mã hóa cho một loại Protein nhỏ là sản phẩm của gen X (HBxAg). Hoạt hóa sao chép này tạo thuận lợi cho sinh sản HBV. Protein X còn có liên quan đến sự điều chỉnh quá trình tăng trưởng của tế bào, cho nên có thể nó có vai trò trong cơ chế sinh ung thư của tế bào gan bị nhiễm HBV.
2.2. Các kháng nguyên của HBV
- HBsAg (Hepatitis B surface Antigen): là kháng nguyên (KN) bề mặt của HBV. HBsAg gồm 2 polypetid có trọng lượng 24.000 và 28.000 mol. HBsAg có một thành phần quyết định KN chung là a đặc điểm nhóm, ngoài ra còn một số KN phụ týp đặc hiệu khác là d, y, w, r, g. Đây là KN xuất hiện sớm nhất trong huyết thanh sau khi nhiễm HBV. Trong viêm gan virus B cấp HBsAg thường đạt đỉnh cao khi có các triệu chứng lâm sàng rồi biến mất sau 2 – 3 tháng. Nếu sau 6 tháng kể từ khi nhiễm mà HBsAg vẫn còn tồn tại trong huyết thanh được coi như mang kháng nguyên mạn tính.
- HBeAg (Hepatitis B envelope Antigen): là Kháng nguyên vỏ xuất hiện sớm thứ hai tiếp sau hoặc đồng thời với HBsAg. Sự có mặt của HBeAg cùng với HBV – DNA trong huyết thanh phản ánh tình trạng đang nhân lên của virus và là thời kỳ lây lan mạnh. HBeAg là kháng nguyên phản ánh chất lượng, còn HBV – DNA là KN phản ánh số lượng của quá trình nhân lên của HBV.
- HBcAg (Hepatitis B core Antigen): là KN lõi của HBV nằm riêng biệt trên bề mặt của nucleocaptid. HBcAg không tồn tại ở dạng tự do mà tập trung chủ yếu trong tế bào gan. Trong huyết thanh HBcAg bị bao bọc bởi HBsAg nên không tìm thấy HBcAg huyết thanh.
- Kháng nguyên Pre-S: Vùng tiền S1 gồm 55 gốc amin và vùng tiền S2 gồm 108 gốc amin chuỗi thẳng của sản phẩm gen S. Vùng tiền S1 và S2 đứng trước gen S trong genome của HBV. Các quyết định KN của vùng tiền S2 có vai trò miễn dịch quan trọng hơn nhiều so với các quyết định KN vùng S. KN Pre-2 cũng định vị trong tế bào gan như HBsAg, có mối liên quan giữa Pre-S2 với nồng độ SGPT. Khi SGPT giảm mạnh là lúc Pre-S2 mất và như vậy Pre-S2 có giá trị tiên lượng trong viêm gan B.
- DNA Polymerase: Nằm trong nucleocapsid nhân của HBV. Nó có thể điều khiển sự sao chép và thay đổi của HBV-DNA. Phát hiện HBV-DNA trong huyết thanh bằng phản ứng khuếch đại gen PCR là biện pháp có giá trị nhất đánh giá tình trạng nhân lên của virus.
- HbxAg: là một protein nhỏ, không có hình dạng nhất định, có thể sao chép cả trong genome và cả trong tế bào. Nhờ có HBxAg, HBV có thể là 1 nhân tố kích thích sự sao chép của các virus khác như HIV. HBxAg luôn thay đổi và cũng được coi là dấu hiệu đặc hiệu và sớm của sự nhân lên của HBV.
2.3. Các thể đột biến của HBV
Những biểu hiện khá đầy đủ về genome của HBV đã cho thấy rõ HBV có 2 thể khác nhau là thể hoang dại (Wild form) và thể đột biến (Mutalion form). Thể đột biến được biểu hiện dưới dạng chứa các protein không điển hình hoặc thay đổi vị trí các gen, ví dụ thiếu protein vỏ hoặc protein của nucleocapsid, hoặc cả hai. Đột biến có thể xảy ra ở vỏ, nhân, trước nhân, ở Protein X và ở DNA Polymerase. Có hai đột biến thường gặp là:
- Đột biến trước nhân (Pre – core mutation): Loại đột biến này được phát hiện lần đầu tiên ở những bệnh nhân viêm gan B với sự có mặt của HBV – DNA và Anti – HBe trong huyết thanh. Vùng trước nhân là nơi mã hóa cho HBeAg. Nếu 1 nucleotid trong vùng này bị thay thể bởi 1 nucleotid khác thì sẽ ngăn cản quá trình tổng hợp HBeAg. Ở những trường hợp này sẽ không có HBeAg, trong khi HBV-DNA có thể được phát hiện với nồng độ cao trong huyết thanh.
- Đột biến trốn thoát (escape mutation): Là loại đột biến trong đó 1 axit amin được thay thế bởi 1 axit amin khác, thường là Arginine thay cho Glycine ở vị trí thứ 145 của thành phần quyết định kháng nguyên a làm cho cấu trúc của HBsAg thay đổi và không bị trung hòa bởi Anti-HBs. Đây là loại đột biến xảy ra ở vùng vỏ của HBV.
Thể đột biến ở vùng nhân được Aye-TT phát hiện năm 1994 trên những bệnh nhân viêm gan virus B ác tính. Ở những bệnh nhân này có sự thay đổi trình tự các axit amin ở vùng giữa nhân và tận cùng 5’ của nhân HBV.
Thể đột biến ở Protein X do Kaneko-M mô tả năm 1995, kết quả là làm thay đổi chức năng của Protein X, qua đó thúc đẩy quá trình nhân lên và trình diện HBV-DNA.
Thể đột biến ở DNA-Polymerase đã được ghi nhận trong những trường hợp có liên quan đến việc sử dụng Lamivudin kéo dài. Thể đột biến này còn được gọi là biến thể YMDD: trình tự axit amin Tryrosine (Y)- Methionine (M)- Asparagine (D)- Asparagine (D) được thay thế bằng YVDD (V – Valine thay cho M) hoặc YIDD (I- Isoleucine thay cho M) ở codon 552. Tuy nhiên biến thể này ít sao chép hơn dạng HBV hoang dại.
2.4. Đáp ứng miễn dịch dịch thể của cơ thể sau khi nhiễm HBV
- Anti – HBc (Hepatittis B core Antibody): là kháng thể có mặt sớm nhất trong đáp ứng miễn dịch của cơ thể sau khi nhiễm HBV, trong đó Anti – HBc – IgM (+) có giá trị chẩn đoán viêm gan virus B cấp. Tuy nhiên ở những bệnh nhân mang HBV mạn tính, trong các đợt kịch phát cấp tính Anti-HBc-IgM cũng có thể xuất hiện. Anti – HBc – IgM tăng cao và kéo dài ở những bệnh nhân viêm gan B mạn tính hoặc người mang HBV mạn tính.
- Anti - HBe (Hepatitis B envelope antibody): là kháng thể xuất hiện thứ hai trong huyết thanh, thường thấy vào giai đoạn cấp tính của bệnh và kéo dài nhiều tháng, nhiều năm. Sự xuất hiện của Anti-HBe là một dấu hiệu chứng tỏ sự nhân lên của virus đã bị khống chế, người bệnh đã bắt đầu hình thành đáp ứng miễn dịch (bước vào giai đoạn chuyển đảo huyết thanh – Seroconversion).
- Anti-HBs (Hepatitis B Surface Antibody): là kháng thể kháng KN bề mặt của HBV. Anti-HBs thường xuất hiện trong huyết thanh sau khi HBsAg biến mất. Sự có mặt cảu Anti-HBs cùng với sự mất đi của HBsAg phản ánh quá trình hồi phục của cơ thể nhiễm virus, cơ thể đã loại trừ được HBV và bệnh nhân đã có đáp ứng miễn dịch đầy đủ đối với bệnh. Cũng có khi HBsAg đã trở về (-) nhưng Anti-HBs chưa xuất hiện, khoảng thời gian này được coi là “thời kì cửa sổ”.
2.5. Sức đề kháng của HBV
HBV có sức đề kháng cao và cao hơn HAV. Virus có thể tồn tại ở nhiệt độ buồng trong vòng 6 tháng, ở 100 độ C trong 20 phút, ở 58 độ C trong 24 giờ. HBsAg rất bền vững, tồn tại 20 năm ở -20 độ C. HBV bị bất hoạt bởi Fomalin 5% trong 12 giờ. Muốn hủy virus hoặc HBsAg thì phải khử trùng rất kĩ (đun sôi 30 phút hoặc sấy khô, hấp ướt).
2.6. Khả năng gây bệnh của HBV
HBV có tính lây nhiễm cao, chỉ với 0,01 – 0,001 ml huyết thanh nhiễm HBV đã có thể lây được bệnh. HBV là tác nhân gây viêm gan virus quan trọng nhất trong các virus viêm gan. Hàng năm trên thế giới có khoảng 380 triệu người nhiễm HBV mạn tính, trong đó khoảng 10% triệu chứng viêm gan cấp, 90% nhiễm virus không có triệu chứng. Trong đó những người lớn mắc bệnh viêm gan B cấp có khoảng 5 – 10% chuyển thành viêm gan mạn. Nguy cơ mắc ung thư gan ở những người mang HBV mạn tính cao gấp 1000 lần so với người không mang HBV.
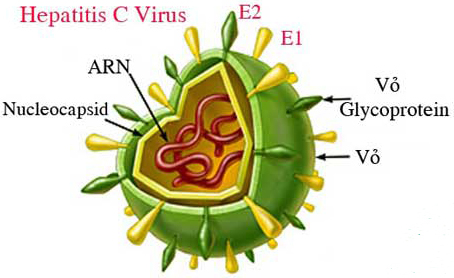
3. Virus viêm gan C (HCV)
HCV do Chou và cộng sự tìm ra năm 1989. Virus thuộc họ Flaviviridae, có 1 lớp vỏ lipoprotein bên ngoài bao bọc 1 capsid 20 mặt có đường kính 55 – 65nm. Hệ gen của virus gồm 1 dây xoắn đơn ARN tính dương, có chứa khoảng 9500 nuleotid. Hệ gen của HCV gồm hai vùng:
- Vùng cấu trúc (structure region) nằm ở đầu 5’ phần không sao mã, gồm các gen: C, E1, E2, P7 là các gen mã hóa cho các protein cấu trúc của virus.
- Vùng không cấu trúc (none structure region) nằm ở đầu 3’ phần không sao mã, có các gen NS2, NS3, NS4, NS5 là các gen mã hóa cho các protein chức năng protease, RNA-polymerase và các peptit tham gia quá trình sao chép virus và cắt đoạn polyprotein.
Đặc tính quan trọng về cấu trúc của gen HCV là:
- Sự đa dạng về gen (tương tự HIV). Ngày nay ít nhất có 6 kiểu gen (týp hoặc genotyp) và 50 týp đã được xác định.
- Các genotyp của HCV có sự khác nhau về độc lực, khả năng gây bệnh và khả năng đáp ứng điều trị bằng Intreron (Genotyp 1 đáp ứng thấp hơn các genotyp khác, 18,1% so với 54,9%).
- Hậu quả về tính đa dạng gen của HCV:
+ Làm virus có khả năng né tránh đáp ứng miễn dịch của vật chủ dẫn đến tỷ lệ nhiễm HCV mạn cao (> 80%).
+ Sau khi khỏi bệnh, cơ thể không có miễn dịch bảo vệ và vẫn có nguy cơ bị tái nhiễm.
+ Việc nghiên cứu sản xuất vacxin phòng bệnh rất khó khăn, hiện chưa có vacxin (do thiếu hệ thống nuôi cấy tế bào thích hợp, do HCV đột biến gen tạo ra chủng virus mới).
.png)
3.2. Sức đề kháng
HCV có sức đề kháng giống với HBV.
3.3. Khả năng gây bệnh
Khoảng 75% số trường hợp sau khi nhiễm HCV không có biểu hiện lâm sàng. Tỷ lệ chuyển từ viêm gan C cấp thành viêm gan C mạn tính khá cao (khoảng 50 – 70%). Nhiễm phối hợp 2 loại HBV và HCV có nguy cơ dẫn tới xơ gan và ung thư gan cao hơn gấp nhiều lần so với viêm nhiễm một loại.
4. Virus viêm gan D (HDV)
Là loại virus không hoàn chỉnh do Rizzetto và cộng sự phát hiện năm 1977. HDV còn gọi là virus delta có hình cầu, đường kính 35 – 37nm. Axit nhân là một sợi ARN nhỏ khoảng nửa triệu Dalton. HDV chỉ có phần nhân ARN còn phần vỏ bọc là HBsAg của HBV (hoặc một Hepadnavirus khác). Do vậy HDV muốn nhân lên phải có HBsAg để làm vỏ mới thành được virus hoàn chỉnh. Chính vì thế mà không bao giờ HDV lại có thể độc lập gây bệnh được. Có thể HDV cùng xâm nhập vào cơ thể người bệnh một lúc với HBV gọi là đồng nhiễm (Coinfection) hoặc nhiễm HDV trên nền một bệnh nhân nhiễm HBV gọi là bội nhiễm (Surinfection). Khi đồng nhiễm HDV và HBV dễ có nguy cơ thành viêm gan ác tính cao. Khi bội nhiễm HDV ở người nhiễm HBV sẽ có nguy cơ thành viêm gan mạn tính.
5. Virus viêm gan E (HEV)
Là một virus chứa ARN không vỏ bọc, kích thước nhỏ, đường kính 32nm, thuộc họ Calcivirus, do Banhamou và cộng sự tìm ra năm 1991. Cho đến nay tất cả các HEV phân lập được đều thuộc 1 týp huyết thanh duy nhất. Virus được phát hiện trong phân, mật ở những người nhiễm bệnh. Ngoài ra, còn có thể phát hiện được HEV trong huyết thanh hoặc trong phân bằng phương pháp PCR.
Phụ nữ có thai, nhất là có thai ba tháng cuối, nếu bị nhiễm HEV dễ có nguy cơ thành viêm gan ác tính, tử vong cao.
6. Virus viêm gan G (HGV)
Là một thành viên thuộc họ Flaviviridae, trong thành phần có 25% sự đồng nhất với HCV nhưng vai trò gây bệnh chưa rõ ràng. Thường trên 70% trường hợp nhiễm HGV không có biểu hiện lâm sàng
Nguồn: Bùi Đại, Nguyễn Văn Mùi, Nguyễn Hoàng Tuấn. http://bacsy.net.vn/Default.aspx?Mod=ViewArticles&ArticlesID=8247