Các nguyên lý tương phản trong MRI
1. Nguyên lý trọng T1
Nói tổng quát, một hình trọng T1 (T1 Weighted Imaging: Weighted có nghĩa là trọng hay thiên về) có thể thu được từ hai chuỗi xung căn bản: chuỗi xung điểm vang spin (chuẩn) và chuỗi xung điểm vang thang từ có nhiễu phá. Các xung đặc hiệu, nhất là các xung xóa mỡ như xung đảo nghịch ngắn (short TI) hay xung bão hòa mỡ cũng có thể được sử dụng kèm với hai chuỗi xung căn bản để tạo ra kết quả mong muốn.
1.1. Chuỗi xung điểm vang spin SE
Cho đến nay đây vẫn là chuỗi xung kinh điển để tạo ra hình ảnh trọng T1 (Hình 1), nhất là đối với các hệ thống chụp ảnh có phần cứng hạn chế. Thời gian TR (ngắn) vào khoảng 600ms còn thời gian TE (ngắn) vào khoảng 20ms. Góc lật dĩ nhiên là 90o. Cần nhớ rằng do hiện tượng suy giảm cảm ứng tự do FID, tín hiệu sẽ ngày càng giảm dần, và vì vậy thời gian TE càng ngắn, chất lượng hình ảnh càng tốt.
.jpg)
Hình 1: Các hình trọng T1 với chuỗi xung điểm vang spin. (a) Hình cắt ngang não (Axial plaine) cho thấy dịch não tủy trong não thất bên (mũi tên) có tín hiệu thấp. (b) Hình cắt dọc đứng (Saggital plaine) qua khớp gối cho thấy mô mỡ dưới da và mỡ trong tủy xương có tín hiệu cao. Sụn chêm có viền sáng nhưng có tín hiệu thấp bên trong (mũi tên).
1.2. Chuỗi xung đảo nghịch IR
Theo cách hiểu thông thường, chuỗi xung đảo nghịch thật ra chỉ là một biến thể của chuỗi xung điểm vang spin, trong đó người ta dùng thêm một xung đảo nghịch 180o trước khi phát xung kích thích một khoảng thời gian TI. Nếu thời đảo TI được chọn khá ngắn, gần bằng với thời gian T1 của mỡ, chuỗi xung khi đó được gọi là chuỗi xung STIR (short TI inversion recovery) mà như chúng ta đã biết nó có tác dụng xóa mỡ.
Về phương diện tương phản, hình ảnh thu được từ chuỗi xung này là một hình trọng T1 ngược chứ thật sự không phải hình trọng T1. Nghĩa là trên hình này, mô có T1 ngắn lại có tín hiệu thấp (màu đen) còn mô có T1 dài lại có tín hiệu cao (màu trắng). Kết quả “ngược đời” này xuất phát từ chỗ mô có T1 dài khi bị đảo ngược 180o sẽ khôi phục chậm hơn. Do vậy vào lúc phát xung kích thích, giá trị tuyệt đối của độ từ hóa dọc của mô có T1 dài vẫn còn lớn (mặc dù có giá trị âm) trong khi mô có T1 ngắn đã khôi phục gần như trở về zero. Khi bị lật ngang bằng xung kích thích, mô có T1 dài sẽ có độ từ hóa ngang lớn hơn, cho ra tín hiệu cao hơn.
Khi chụp ở não, chuỗi xung STIR thường được in “âm bản” khiến cho vùng trắng được in thành đen và ngược lại. Nghĩa là khi đó hình trọng T1 ngược trở thành hình trọng T1 thực sự (Hình 2).
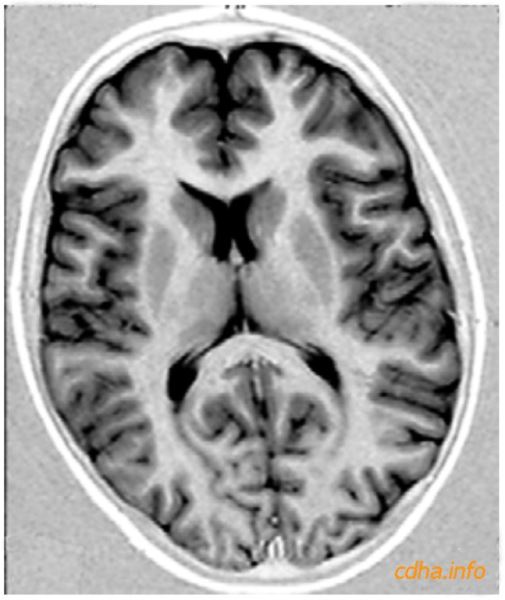
Hình 2: Hình trọng T1 chụp bằng chuỗi xung STIR và in âm bản phân định rất rõ cấu trúc chất xám và chất trắng. Để ý vùng nền của không khí xung quanh đầu bệnh nhân lúc chụp trên hình này có màu xám trắng, trong khi đó trên các phim thông thường đều có màu đen.
1.3. Chuỗi xung điểm vang thang từ có nhiễu phá GRE
Các chuỗi xung điểm vang thang từ thường dùng thời gian TR ngắn kèm với góc lật nhỏ hơn 90o. Khi TR ngắn hơn T2 của một mô nào đó trong vùng cần chụp thì tại thời điểm phát xung kích thích tiếp theo, độ từ hóa ngang vẫn còn tồn tại. Độ từ hóa ngang còn dư lại làm tăng đặc thù trọng T2 và làm giảm đặc thù trọng T1 của hình.
Để bảo đảm chất lượng của một hình trọng T1, trong chuỗi xung điểm vang thang từ có nhiễu phá (spoiled gradient echo), người ta phải nhiễu phá độ từ hóa ngang còn dư lại này bằng một xung hoặc một thang từ nhiễu phá. Khi đó ở lần kích thích tiếp theo, độ từ hóa ngang bị mất hoàn toàn hoặc chỉ còn rất ít. Nếu chọn lựa các tham số TR, TE và góc lật một cách thích hợp, chúng ta có thể thu được một hình trọng T1 rất đặc thù (Hình 3).
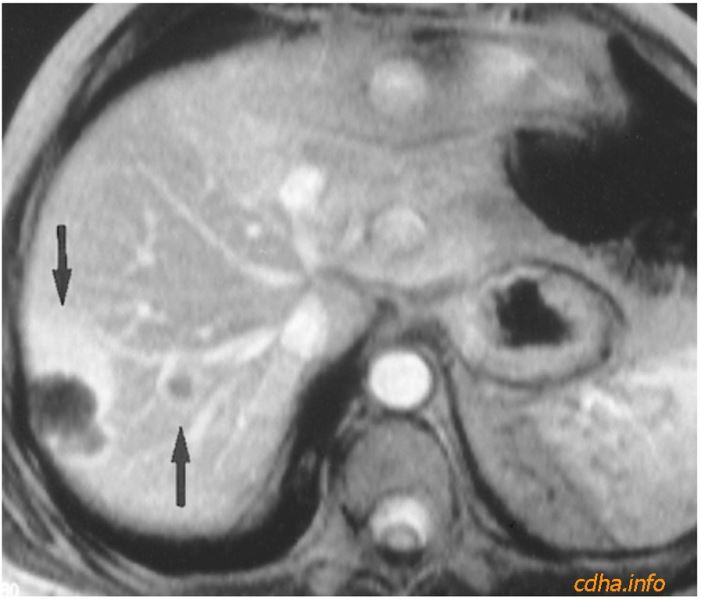
Hình 3: Hình trọng T1 được thực hiện trong thì động mạch sau khi tiêm Gado cho thấy nhiều tổn thương di căn của gan (mũi tên).
Chuỗi xung điểm vang thang từ có nhiễu phá có thể được thực hiện kèm với kỹ thuật chụp đa lớp cắt hoặc chụp ba chiều. Mỗi kỹ thuật này đều có những ưu điểm riêng vốn có của chúng, và khi bổ túc vào chuỗi xung này chúng làm tăng hiệu quả của chuỗi xung lên rất nhiều.
Cũng cần nhắc lại ở đây rằng các tên thương mại khá phổ biến của chuỗi xung điểm vang thang từ có nhiễu phá là FLASH (hãng Siemens), spoiled GRASS hay SPRG (hãng GE).
2. Nguyên lý trọng T2
So với các hình trọng T1 thường chỉ được tạo ra bằng cách dùng các chuỗi xung điểm vang spin và điểm vang thang từ có nhiễu phá, các hình trọng T2 có thể được tạo ra bằng nhiều kỹ thuật hơn, mặc dù một số kỹ thuật thực sự cho hình trọng T2/T1 chứ không đơn thuần trọng T2. Một hình trọng T2/T1 là hình có tín hiệu cao đối với các mô có T2 dài hoặc có T1 ngắn.
2.1. Chuỗi xung điểm vang spin SE
Sử dụng chuỗi xung điểm vang spin để tạo ra một hình trọng T2 là một kỹ thuật kinh điển. Với thời gian TR dài và TE dài, tín hiệu của các mô có T2 ngắn hầu như đã mất hết do hiện tượng suy giảm cảm ứng tự do FID, chỉ còn lại tín hiệu của các mô có T2 dài, tạo ra một hình có độ tương phản dựa vào đặc thù thời gian T2 của các mô.
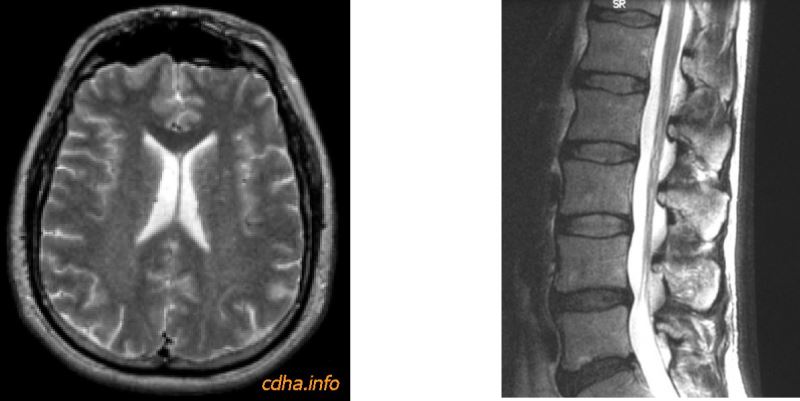
Hình 4: Hình trọng T2 chụp bằng chuỗi xung điểm vang spin cho não (bên trái) và cột sống (bên phải) cho thấy dịch não tủy có tín hiệu cao (màu trắng) vì có thời gian T2 rất dài.
2.2. Chuỗi xung điểm vang thang từ GRE
Chúng ta đã biết rằng chuỗi xung điểm vang thang từ không dùng xung tái lập 180o. Thay vì thế nó sử dụng một thùy hồi pha để điều chỉnh tình trạng lệch pha do thùy khử pha gây ra. Ở điểm này, thùy hồi pha có tác dụng kém hơn xung tái lập 180o. Nó không có khả năng điều chỉnh tình trạng lệch pha gây ra do tình trạng không đồng nhất của từ trường cục bộ hoặc do độ xê dịch hóa học. Điều này nói lên rằng chuỗi xung điểm vang thang từ dễ bị ảnh hưởng của tình trạng không đồng nhất của từ trường cục bộ hoặc độ xê dịch hóa học, dẫn đến tình trạng mất tín hiệu cục bộ.
Khi có xuất huyết hoặc vôi hóa, tính chất thuận từ của sắt (từ các sản phẩm của quá trình phân hủy hồng cầu trong khối máu xuất huyết) và canxi sẽ làm cho từ trường cục bộ trở nên kém đồng nhất. Vận dụng đặc điểm nhạy với tình trạng không đồng nhất của từ trường cục bộ của chuỗi xung điểm vang thang từ, người ta thường dùng nó để xác định chẩn đoán (Hình 5).
Cũng cần nhắc lại rằng tính không đồng nhất của từ trường và độ xê dịch hóa học vốn luôn hiện diện trong mọi mô. Chúng làm cho thời gian suy giảm tín hiệu FID thực tế (thời gian T2*) ngắn hơn thời gian suy giảm lý thuyết (thời gian T2). Chuỗi xung điểm vang thang từ vì thế được xem là chuỗi xung tạo ra hình trọng T2* thay vì trọng T2. Vì vậy có đôi khi người ta cũng gọi chuỗi xung điểm vang thang từ là chuỗi xung T2* (các tác giả Pháp).
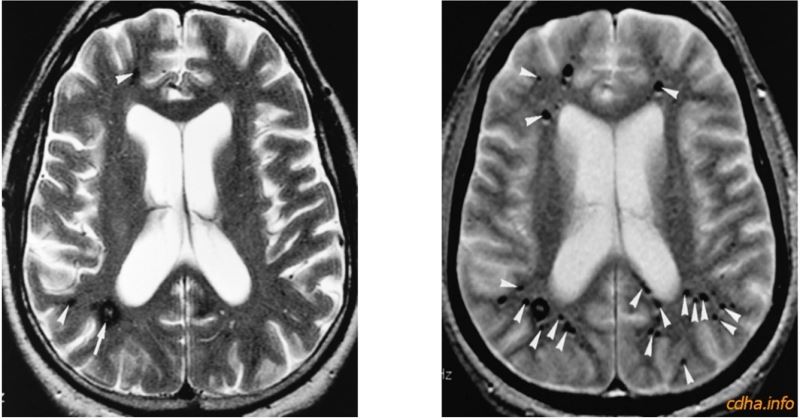
Hình 5: Hình trọng T2 chụp bằng chuỗi xung điểm vang spin nhanh (bên trái) cho thấy nhiều tổn thương xuất huyết (mũi tên). Thế nhưng khi chụp bằng chuỗi xung điểm vang thang từ (bên phải), người ta phát hiện ra khá nhiều tổn thương nhỏ (đầu mũi tên).
2.3. Chuỗi xung điểm vang thang từ không nhiễu phá
Các chuỗi xung điểm vang thang từ không nhiễu phá nói chung đều sinh ra các hình trọng T2/T1. Do thời gian TR ngắn, mô có T1 ngắn khôi phục độ từ hóa dọc được nhiều hơn; do không nhiễu phá độ từ hóa ngang còn dư, mô có T2 dài có độ từ hóa ngang lớn hơn. Cả mô có T1 ngắn lẫn mô có T2 dài như vậy đều có tín hiệu cao trên hình, cho ra hình trọng T2/T1.
Thực tế, thời gian T1 và T2 của các mô thường song hành với nhau, nghĩa là mô có T1 dài cũng có T2 dài và ngược lại. Vì vậy độ tương phản trên các hình trọng T2/T1 thường không rõ. Chẳng hạn mô gan có T1 ngắn nên sẽ có tín hiệu cao hơn đa số các tổn thương gan với T1 dài trên hình trọng T1; ngược lại các tổn thương gan thường có T2 cũng dài nên có tín hiệu cao hơn gan trên hình trọng T2. Thế nhưng trên hình trọng T2/T1, cả hai đều có tín hiệu cao, không có được một độ tương phản rõ rệt giữa chúng.
Các chuỗi xung đầu tiên loại này thường được gọi với tên thương mại là FISP (hãng Siemens) và GRASS (hãng GE). Gần đây hơn, chuỗi xung SSFP (Steady State Free Precession) được thiết kế với thời gian TR và TE cực ngắn (3 và 1 ms) có nhiều ứng dụng lâm sàng, đặc biệt đối với vùng bụng và tim mạch. Tên thương mại khá thông dụng của nó là trueFISP (Siemens).
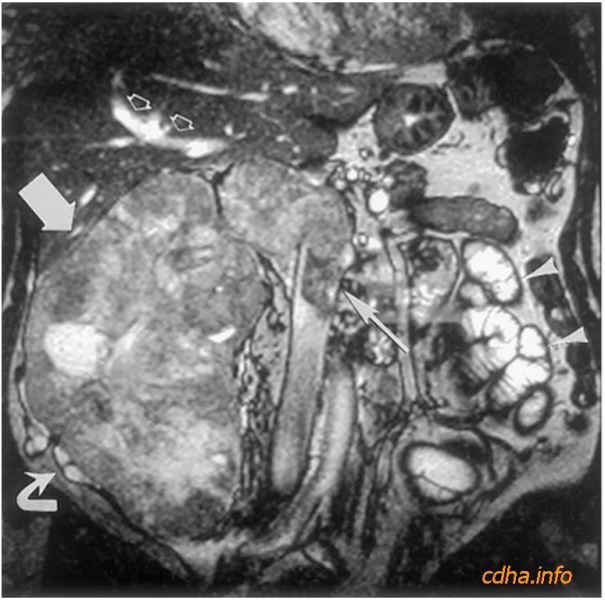
Hình 6: Hình dọc trán chụp bằng chuỗi xung true FISP thấy rất rõ một khối u lớn nằm ở vùng hố thận phải (mũi tên lớn) được chẩn đoán là carcinoma thận phải.
2.4. Chuỗi xung điểm vang spin nhanh FSE
Từ Phần 6 chúng ta đã biết rằng các chuỗi xung nhiều điểm vang cho ra hình trọng T2, đặc biệt khi thời vang hiệu dụng TEef dài. Đối với các chuỗi xung một phát (single-shot), toàn bộ các hàng trong k-không gian đều được lấy mẫu qua một lần phát xung, do vậy không có TR hoặc có thể xem TR dài vô tận. Đối với các chuỗi xung nhiều phát (multishot), mỗi thời khoảng TR sẽ ghi nhận tín hiệu cho nhiều hàng trong k-không gian, mỗi hàng được lấy mẫu từ một điểm vang trong xâu điểm vang.
Trong trường hợp thông thường, hiện nay người ta có xu hướng thay chuỗi xung SE chụp hình trọng T2 bằng chuỗi xung chụp nhanh nhiều phát. Hiệu quả của chuỗi xung chụp nhanh rõ ràng là hơn hẳn dù độ tương phản và chất lượng hình nói chung có giảm bớt một ít.
Nếu phải chụp thật nhanh, người ta có thể dùng chuỗi xung một phát SSFSE (single-shot fast spin echo) mà tên thương mại rất phổ biến của nó là HASTE (half-Fourier acquisition single shot turbo spin echo). Các chuỗi xung có tên turbo đều là chuỗi xung nhanh của của hãng Siemens: turboSE, turbo- FLASH, turboGSE, turboIR. Như tên gọi của nó cho biết, HASTE sử dụng một chiến lược điền dữ liệu vào k-không gian gọi là kỹ thuật nửa-Fourier (half-Fourier). Kỹ thuật này tận dụng tính đối xứng của k-không gian bằng cách thay vì điền hết mọi hàng trong đó, nó chỉ thực hiện điền hơn một nửa số hàng cần thiết; số hàng còn lại sẽ được máy tính “nội suy” và lấp đầy vào. Nếu chọn thời vang hiệu dụng TEef thật dài, hình thu được hầu như chỉ có tín hiệu của nước. Đặc điểm này được sử dụng để chụp đường mật và ống tụy (Hình 7) và gọi là mật tụy đồ cộng hưởng MRCP (MR Cholangiopancreatography).
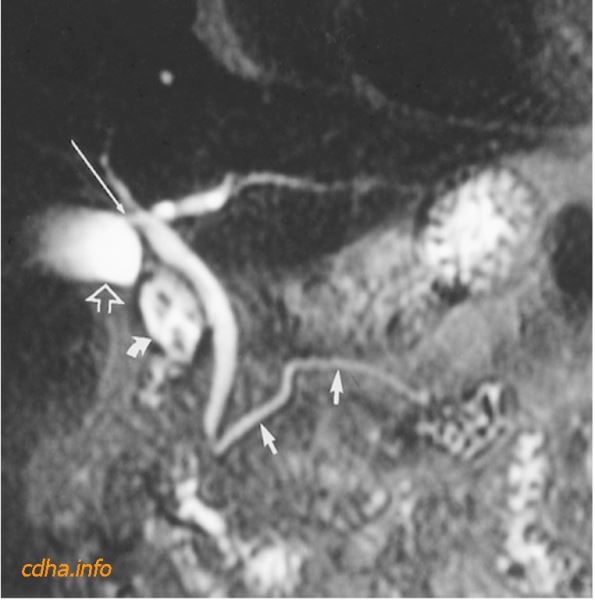
Hình 7: Hình MRCP chụp bằng kỹ thuật HASTE cho thấy rõ túi mật (mũi tên rỗng), ống gan trái, ống mật chủ, tá tràng (mũi tên cong), ống tụy (mũi tên ngắn). Ống gan phải bị che khuất chỉ thấy một phần (mũi tên dài).
Đặc biệt hơn, chuỗi xung điểm vang spin nhanh có thể sử dụng thêm một xung đảo nghịch 180o trước khi phát xung kích thích, cho phép xóa mỡ (chuỗi xung STIR) hoặc xóa dịch (chuỗi xung FLAIR). Chúng ta cần nhớ rằng chuỗi xung FLAIR vốn đã tạo ra hình trọng T2 khi được chụp bằng kỹ thuật thông thường (dùng điểm vang spin), trong khi đó chuỗi STIR thực chất cho ra hình trọng T1 ngược. Khi sử dụng chuỗi xung STIR với kỹ thuật chụp hình nhanh (điểm vang spin nhanh) và với thời vang TEef đủ dài, chuỗi xung STIR nhanh này cho ra hình trọng T2 (Hình 8) mặc dù vẫn biểu hiện một phần đặc tính trọng T1 vốn có của mình.
2.5. Chuỗi xung điểm vang đồng phẳng
Giống như kỹ thuật điểm vang spin nhanh, các chuỗi xung điểm vang đồng phẳng EPI về cơ bản cũng tạo ra các hình trọng T2. Khác biệt chủ yếu của chuỗi xung điểm vang đồng phẳng so với chuỗi xung điểm vang spin nhanh là điểm vang được tạo ra trong chuỗi xung đồng phẳng là điểm vang thang từ, không phải điểm vang spin. Tuy nhiên người ta cũng tìm cách phối hợp chuỗi xung điểm vang đồng phẳng EPI với điểm vang spin SE bằng cách thực hiện một xung tái lập 180o vào thời điểm TEef/2. Nhờ xung tái lập này, hình ảnh thu được ít bị ảnh hưởng bởi tình trạng không đồng nhất của từ trường cục bộ và độ xê dịch hóa học vốn là một đặc trưng của các chuỗi xung điểm vang thang từ.
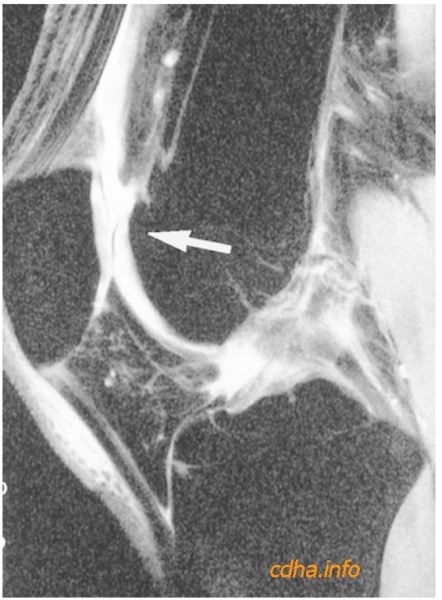
Hình 8: Hình chụp đứng dọc khớp gối với chuỗi xung STIR nhanh (TR/TEef/ TI, 5000/30/150) xóa rất tốt mỡ của tủy xương và cho thấy rõ tụ dịch trên xương bánh chè (mũi tên) bằng tín hiệu rất cao.
3. Nguyên lý trọng đậm độ proton
Hiện tại, ngoài hai chuyên khoa thần kinh và cơ xương khớp, các hình trọng đậm độ proton (proton density) rất ít được dùng. Kỹ thuật chủ yếu vẫn là chuỗi xung điểm vang spin kinh điển; một số trường hợp có thể dùng kỹ thuật điểm vang spin nhanh. Trong thực tế, hình trọng đậm độ proton thường được chụp chung với hình trọng T2 bằng kỹ thuật điểm vang kép (double-echo hay dual-echo), mỗi điểm vang tạo ra một hình. Với kỹ thuật này, sau mỗi xung kích thích 90o, người ta phát hai xung tái lập 180o tại hai thời điểm khác nhau trong khoảng thời gian TR sao cho điểm vang thứ nhất có thời vang TE khá ngắn dành cho hình trọng đậm độ proton còn điểm vang thứ hai có thời vang TE khá dài dành cho hình trọng T2.
Trong thực tế lâm sàng, hình trọng đậm độ proton rất có giá trị khi cần đánh giá các cấu trúc có tín hiệu thấp như mô sợi. Đặc biệt, hình trọng đậm độ proton được xem là hình có độ nhạy tốt nhất đối với các trường hợp rách sụn chêm (Hình 9).
4. Nguyên lý trọng dòng chảy
Nguyên lý và kỹ thuật chụp dòng chảy đã được chúng ta tìm hiểu khá chi tiết trong Phần 8. Tuy nhiên để cho độc giả có được một cái nhìn toàn cảnh từ góc độ nguyên lý tương phản cộng hưởng từ, chúng ta sẽ lược qua một số điểm mấu chốt có liên quan đến tín hiệu của các dòng chảy.
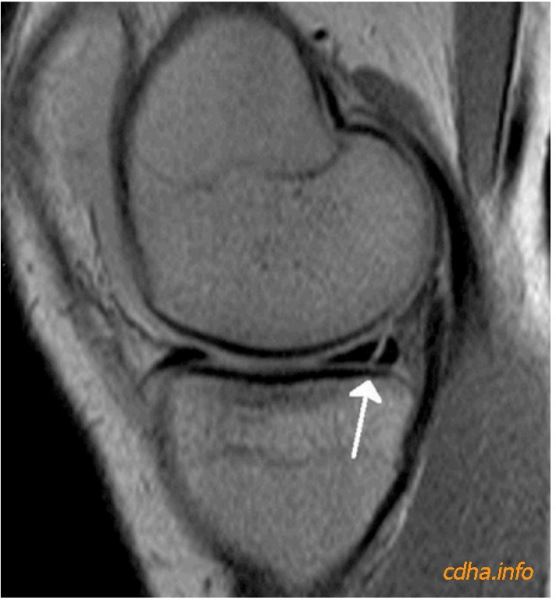
Hình 9: Hình đứng dọc trọng đậm độ proton cho thấy rất rõ một đường rách ở sừng sau của sụn chêm trong (mũi tên) kéo dài từ mặt khớp trên đến mặt khớp dưới.
4.1. Độ tương phản do thuốc
Các thuốc tương phản từ đa số đều dùng theo đường tiêm tĩnh mạch với tác dụng chủ yếu là làm giảm rõ rệt thời gian T1 và T2 của dòng máu và của các mô “bắt thuốc”, dù rằng mức độ có khác nhau tùy theo từng loại thuốc.
Tác dụng làm giảm thời gian T1 biểu hiện ra khi được chụp bằng các chuỗi xung “trọng T1”, chẳng hạn với chuỗi xung điểm vang spin có cả TR và TE đều ngắn, khi đó mạch máu và các mô bắt thuốc sẽ có tín hiệu cao. Tác dụng làm giảm thời gian T2 biểu hiện bằng tình trạng giảm tín hiệu khi được chụp bằng các chuỗi xung “trọng T2”. Tác dụng này trong thực tế không dùng để đánh giá mạch máu mà chỉ được sử dụng để làm giảm T2 của các mô, cho phép chụp các hình trọng T2 hoặc T2*. Thí dụ các chất SPIO có thể được các tế bào Kuffer trong gan bắt giữ, làm giảm tín hiệu của nhu mô gan so với tổn thương và các mô xung quanh (Hình 10).
Về mặt huyết động học, nói chung trong khoảng thời gian 30 giây sau tiêm, thuốc chủ yếu tồn tại trong động mạch (thì động mạch). Trong khoảng 30 giây tiếp theo, thuốc lan tỏa qua mao mạch rồi đến tĩnh mạch (thì hồ máu). Sau thời điểm 60 giây, thuốc đã ngấm qua thành mao mạch (ngoại trừ mao mạch hệ thần kinh và tinh hoàn) để vào khoang gian bào nhưng nhìn chung vẫn tiếp tục tồn tại trong hồ máu (thì ngoại bào). Từ thời gian này trở về sau, các thuốc đặc hiệu với tế bào (tế bào gan, tế bào hệ lưới nội mô, vân vân) mới có thể vào được nội bào và có tác dụng.
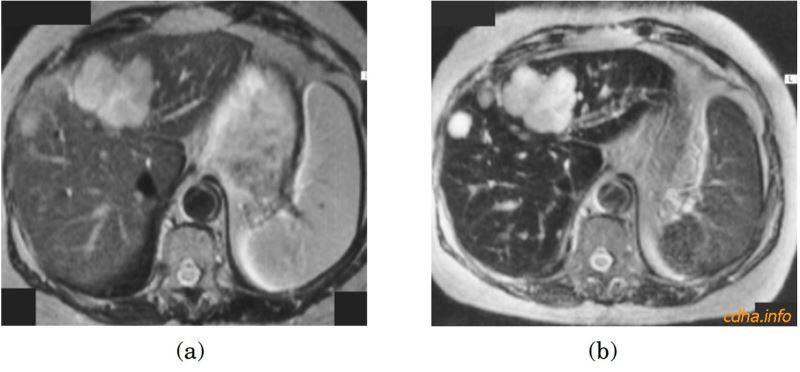
Hình 10: (a) Hình cắt ngang bụng trọng T2 không tiêm thuốc cho thấy một tổn thương rất lớn và các tổn thương nhỏ không rõ bờ ở gan. (b) Sau khi tiêm ferumoxide (AMI-25), trên hình trọng T2 tín hiệu của nhu mô gan giảm rõ, làm tăng độ tương phản giữa nhu mô và các tổn thương.
Do những đặc điểm về huyết động học nêu trên, thời điểm chụp sau khi tiêm thuốc có ảnh hưởng rất lớn đến khả năng làm thay đổi thời gian T1 và T2 của thuốc tương phản. Nếu muốn đánh giá tình trạng động mạch, chúng ta cần chụp ở thì sớm (thì động mạch), tốt nhất không nên để quá 20 giây sau tiêm. Khi để trễ hơn, chúng ta có thể thấy cả tĩnh mạch (thì hồ máu). Đánh giá khả năng “bắt thuốc” của mô cần thực hiện ở thì ngoại bào, tốt nhất sau tiêm 2 phút. Với các thuốc đặc hiệu tế bào, thời gian chụp có thể lâu hơn và kéo dài nhiều giờ. Thời điểm bắt đầu chụp có thể từ 10 đến 30 phút sau tiêm.
Trong trường hợp đặc biệt hơn, một số tổn thương có tính chất huyết động khá đặc thù, biểu hiện ở tốc độ và cách thức “bắt thuốc”, kể cả tốc độ và cách thức “xả thuốc”. Khi đó, một phương thức chụp “động” (dynamic) sẽ thích hợp hơn. Chẳng hạn để đánh giá một tổn thương nghi ngờ là hemangioma ở gan, người ta tiêm thuốc tương phản nhóm chelate gado rồi chụp các hình trọng T1 bằng chuỗi xung điểm vang thang từ: chụp một hình ngay trước khi tiêm rồi chụp lập lại các hình ở thì động mạch (khoảng 30 giây sau tiêm), thì hồ máu hay thì tĩnh mạch cửa (khoảng 30 giây nữa) và thì ngoại bào hay thì cân bằng (khoảng 2 đến 3 phút sau tiêm). Kỹ thuật chụp động này cho phép đánh giá tính chất “bắt thuốc” và “xả thuốc” của tổn thương (Hình 11).
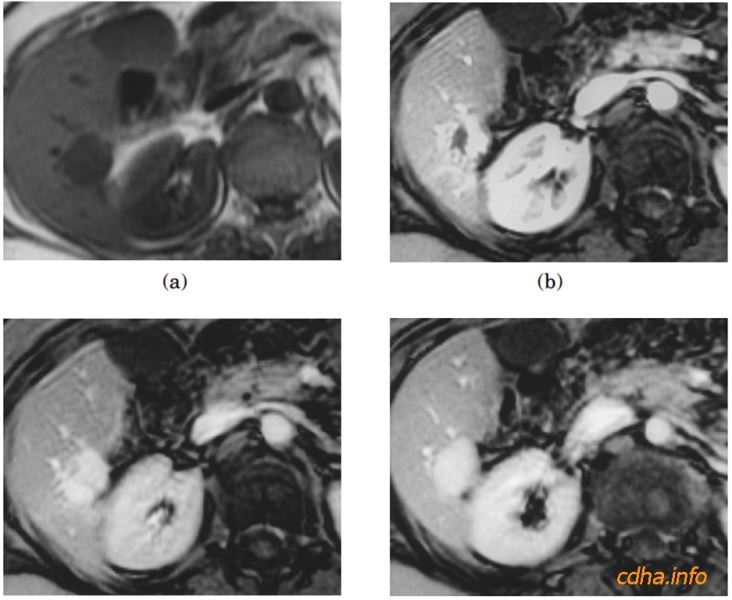
Hình 11: Chuỗi hình chụp động trọng T1 đánh giá một tổn thương nghi ngờ hemangioma ở gan. (a) Chụp ngay trước tiêm (b-d) Các hình chụp động sau tiêm ở thì động mạch (b), thì tĩnh mạch cửa (c) và thì cân bằng (d).
4.2. Độ tương phản do hiệu ứng dòng chảy
Ngoài cách dùng thuốc để tạo ra độ tương phản, một cách làm có phần tương tự như dùng thuốc cản quang trong CT và X quang quy ước, cộng hưởng từ còn có thể sử dụng ngay sự chuyển động của dòng máu để có được một độ tương phản nhất định so với các mô đứng yên. Đặc biệt hơn, máu chảy trong lòng mạch không chỉ sáng tương tự như khi dùng thuốc tương phản mà còn có thể tối hơn so với các mô đứng yên. Hiệu ứng tạo ra hình ảnh máu tối là hiệu ứng trống dòng (flow void effect) trong khi đó hiệu ứng tạo ra hình ảnh máu sáng là hiệu ứng nội dòng (inflow effect).
Hiệu ứng trống dòng thường xảy ra khi chụp bằng chuỗi xung điểm vang spin (SE hoặc FSE) cho những dòng máu chảy chậm, với tín hiệu được ghi nhận tại một thời vang TE hoặc TEef khá dài sau xung kích thích. Trong tình huống này, máu bị lệch pha nhiều nhưng do hầu như đã chảy ra khỏi lớp cắt đang chụp nên không nhận được xung tái lập 180o, trong khi đó khối máu mới thay thế lại chưa nhận được xung kích thích. Kết quả là tại thời điểm đo tín hiệu TE hoặc thời điểm ghi nhận tín hiệu cho các hàng gần trung tâm của k-không gian (TEef), dòng máu chảy có tín hiệu rất thấp, cho ra hình ảnh máu đen khiến chúng ta có cảm giác như trong lòng mạch không có gì (trống dòng).
Hiệu ứng nội dòng xảy ra khi một khối máu mới chưa bị bão hòa chảy vào vùng đang được chụp hình. Ở thời điểm này, các mô đứng yên xung quanh đã nhận được nhiều loại xung và thang từ khác nhau, dẫn đến tình trạng chúng bị bão hòa khá nhiều. Do vậy khi được kích thích ở lần tiếp theo, tín hiệu của các mô đứng yên so với tín hiệu của khối máu mới sẽ thấp hơn. Nếu được chụp bằng một kỹ thuật thích hợp, thường là một chuỗi xung nhanh, dòng máu đang chảy sẽ có tín hiệu cao hơn hẳn so với mô đứng yên xung quanh (Hình 12).

Hình 12: Hình minh họa cho hiệu ứng nội dòng.
Ngoài hiệu ứng nội dòng, người ta còn có thể dùng độ chênh lệch pha hay độ tương phản pha (phase contrast) để tạo ra hình ảnh máu sáng, cho phép đánh giá được cả tốc độ chảy của dòng máu. Muốn vậy, người ta cần chụp vùng đang khảo sát ở hai thời điểm khác nhau. Khi so sánh dữ liệu của hai thời điểm này, các mô đứng yên không có sự khác biệt về pha còn dòng máu chảy có một độ chênh lệch rõ rệt. Độ chênh lệch zero của các mô đứng yên hiển thị thành hình tối còn độ chênh lệch khác zero của dòng máu đang chảy hiển thị thành hình sáng.
5. Nguyên lý trọng khuếch tán
Ở góc độ triết học, chuyển động là một thuộc tính vốn có của sự vật. Ở góc độ sinh học, chuyển động biểu thị các hoạt động chức năng của cơ thể. Các quá trình sinh lý xảy ra trong cơ thể, từ mức độ đại thể như các hoạt động hít vào, thở ra của phổi hay hoạt động co bóp của tim đến các mức độ vi thể như các quá trình trao đổi chất ở tế bào đều những biểu hiện cụ thể của sự chuyển động.
Nhờ khả năng “nhạy cảm” với sự chuyển động, cộng hưởng từ đã được kỳ vọng như một phương tiện giúp chúng ta đánh giá được chức năng của các bộ phận, nghĩa là các quá trình hoạt động của chúng. Mặc dù đã được đặt ra từ lâu nhưng do những hạn chế về phần cứng và kỹ thuật, kỳ vọng này gần đây mới bắt đầu trở thành hiện thực, mở ra một lĩnh vực mới với tên gọi là chụp cộng hưởng từ chức năng fMRI (functional MRI). Trong phần này và phần tiếp theo, chúng ta sẽ rảo qua hai kỹ thuật cơ sở của chụp cộng hưởng từ chức năng, đó là kỹ thuật khuếch tán (diffusion) và kỹ thuật tưới máu (perfusion).
5.1. Hiện tượng khuếch tán
Chắc hẳn nhiều người trong chúng ta còn nhớ từ những năm học phổ thông rằng khi ở trạng thái lỏng (thể lỏng), các phân tử nước chuyển động không ngừng và hỗn loạn theo mọi hướng mà chúng ta gọi là chuyển động Brown. Theo thời gian, chúng có thể tản mác ra khắp môi trường. Nói một cách “hàn lâm” hơn, chúng ta bảo rằng chúng khuếch tán khắp nơi. Tốc độ khuếch tán phụ thuộc vào nhiều yếu tố của môi trường, đặc biệt là độ nhớt và nhiệt độ môi trường.
Để lượng hóa khái niệm khuếch tán, người ta sử dụng một con số gọi là hệ số khuếch tán (diffusion coefficient) với đơn vị là diện tích/thời gian. Hệ số này cho biết diện tích mà một phân tử chất lỏng (ở đây là nước) có thể dịch chuyển (khuếch tán) trong một đơn vị thời gian. Trong thực tế, hệ số khuếch tán được tính bằng đơn vị cụ thể mm2/giây (mm2/sec). Thí dụ ở nhiệt độ 37oC, nước nguyên chất có hệ số khuếch tán là 0,003 mm2/sec.
Trong cơ thể, nước cũng khuếch tán khắp nơi, nghĩa là các phân tử nước cũng luôn di chuyển không ngừng và hỗn loạn theo mọi hướng bằng chuyển động Brown. Tuy nhiên chuyển động Brown của nước trong cơ thể bị hạn chế bởi các cấu trúc giải phẫu vi thể và các phân tử lớn có mặt trong mỗi mô. Khi này, thay vì dùng hệ số khuếch tán, người ta đưa ra khái niệm hệ số khuếch tán biểu kiến ADC (apparent diffusion coefficient). Hệ số ADC thay đổi tùy theo cấu trúc và tình trạng bệnh lý của mỗi mô. Mô có hệ số ADC càng lớn, khả năng khuếch tán của nước trong mô càng mạnh.
5.2. Tính dị hướng
Không giống như hiện tượng khuếch tán trong môi trường tự do, hiện tượng khuếch tán của nước ở các mô cơ thể không có tính đẳng hướng (isotropy) mà có tính dị hướng (anisotropy), nghĩa là chúng không khuếch tán giống nhau theo mọi hướng. Ở mô sợi hoặc các mô có mức độ tổ chức cao như gân, cơ, chất trắng, các phân tử lớn thường được sắp xếp theo một hướng nhất định, hạn chế khả năng khuếch tán của nước theo một hướng nào đó và làm cho nước “có khuynh hướng” khuếch tán theo một hướng khác nhiều hơn. Hệ số ADC do vậy vừa biểu thị tốc độ khuếch tán (độ lớn của hệ số) vừa biểu thị hướng khuếch tán theo ba chiều không gian x, y, z. Thông tin độ lớn của ADC được sử dụng để tạo ra một hình cộng hưởng từ có tên là bản đồ ADC (ADC map).
Ở não, người ta nhận thấy rằng hiện tượng khuếch tán có khuynh hướng xảy ra dọc theo hướng sợi trục của chất trắng dù rằng nguyên nhân đích xác của nó chưa được giải thích thấu đáo. Hình 13 minh họa khuynh hướng khuếch tán này.
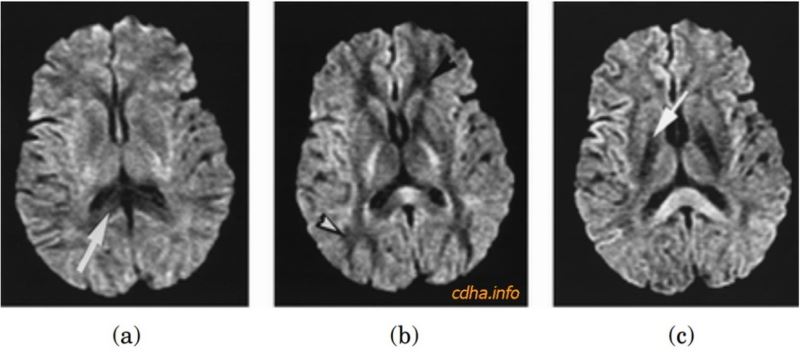
Hình 13: Các hình chụp ngang não với hệ số nhạy khuếch tán b = 1000 sec/mm2 với thang từ khuếch tán được áp dụng theo một trục. Theo chiều áp dụng của thang từ, bó sợi chất trắng dọc theo trục đó bị giảm tín hiệu (các mũi tên trong mỗi hình). (a) Thang từ được áp dụng theo trục x từ phải sang trái: thể chai có tín hiệu thấp. (b) Thang từ được áp dụng theo trục y từ trước ra sau: chất trắng vùng trán và đính giảm tín hiệu. (c) Thang từ được áp dụng theo trục z (đứng) từ trên xuống dưới: bó vỏ gai (bao trong) giảm tín hiệu.
5.3. Đặc tính cộng hưởng từ khuếch tán
Do chuyển động Brown của các phân tử nước, hiện tượng khuếch tán cũng là một nguyên nhân gây ra tình trạng lệch pha của các proton dưới tác dụng của các xung và các thang từ trong quá trình chụp hình. Tình trạng lệch pha này tỷ lệ thuận với cường độ và thời gian áp đặt thang từ. Thế nhưng các xung tái lập và các thùy hồi pha lại không điều chỉnh được nguyên nhân lệch pha do khuếch tán vì tình trạng hỗn loạn vốn có của chuyển động Brown.
Như vậy, ngoài nguyên nhân hồi giãn ngang trong khoảng thời gian T2 làm mất dần tín hiệu vốn tồn tại ngay cả khi không có các thang từ, nguyên nhân khuếch tán làm mất tín hiệu sẽ xảy ra khi có tác dụng của các thang từ. Nghĩa là lúc này, cường độ tín hiệu cần phải được tính theo hai tham số độc lập nhau: thời gian T2 và hệ số khuếch tán.
May mắn là trong những tình huống bình thường, các thang từ được sử dụng có cường độ nhỏ nên ảnh hưởng của hiện tượng khuếch tán đối với tình trạng mất tín hiệu có thể bỏ qua. Khi sử dụng các thang từ có cường độ mạnh được thiết kế để đánh giá hiện tượng khuếch tán, ảnh hưởng lệch pha do khuếch tán mới bộc lộ. Khi đó chúng ta cần đánh giá cả ảnh hưởng của T2 lẫn của hiện tượng khuếch tán.
5.4. Hệ số nhạy cảm khuếch tán
Để đánh giá được tình trạng khuếch tán của nước trong các mô cơ thể, người ta sử dụng các thang từ chuyên biệt gọi là thang từ khuếch tán (diffusion gradient). Mức độ nhạy cảm của các chuỗi xung đối với hiện tượng khuếch tán tùy thuộc vào cường độ và thời gian áp dụng thang từ khuếch tán. Khi đó, để điều chỉnh tác dụng của thang từ khuếch tán, người ta sử dụng hệ số nhạy khuếch tán b (diffusion sensitivity factor) được tính bằng đơn vị là giây/mm2 (sec/mm2). Giá trị b = 0 biểu thị chuỗi xung không nhạy khuếch tán, nghĩa là một chuỗi xung bình thường không nhằm đo đạc mức độ khuếch tán. Giá trị nhạy khuếch tán thường được sử dụng trong lâm sàng thay đổi từ 500 đến 1500 sec/mm2.
5.5. Kỹ thuật và các hình khuếch tán
Với những đặc tính đã nêu ở trên, hiện tượng khuếch tán trong cơ thể vừa là hiện tượng vật lý vừa là hiện tượng sinh lý. Quá trình này xảy ra ở mức phân tử với một tốc độ rất nhanh nên để có thể đo được hệ số ADC, người ta hay sử dụng các chuỗi xung điểm vang đồng phẳng EPI vì khả năng chụp nhanh của chúng. Bộ hình kinh điển để đánh giá hiện tượng khuếch tán gồm có ba nhóm: hình trọng T2, hình trọng khuếch tán DW và hình bản đồ ADC.
- Các hình trọng T2 (T2W) được chụp bằng chuỗi xung điểm vang đồng phẳng và được dùng làm cơ sở để so sánh và tạo lập hình bản đồ ADC. Trong bộ xung chụp hình khuếch tán, hình trọng T2 là hình được chụp với giá trị b = 0.
- Các hình trọng khuếch tán DW (diffusion-weighted) được thực hiện bằng cách trước tiên áp dụng thang từ khuếch tán theo mỗi trục x, y, z để có được ba hình trọng khuếch tán DW theo mỗi trục (Hình 13). Sau đó “nhân” tín hiệu của ba hình khuếch tán theo mỗi trục rồi lấy căn bậc ba của tích này, cho ra giá trị tín hiệu được dùng để tạo ra hình trọng khuếch tán DW (Hình 14). Hình trọng khuếch tán DW này chưa loại bỏ yếu tố làm mất tín hiệu do thời gian hồi giãn ngang T2 nên vẫn còn biểu hiện một phần đặc thù trọng T2. Chẳng hạn độ tương phản giữa chất xám chất trắng trên hình trọng khuếch tán DW chính là độ tương phản của chúng trên hình trọng T2.
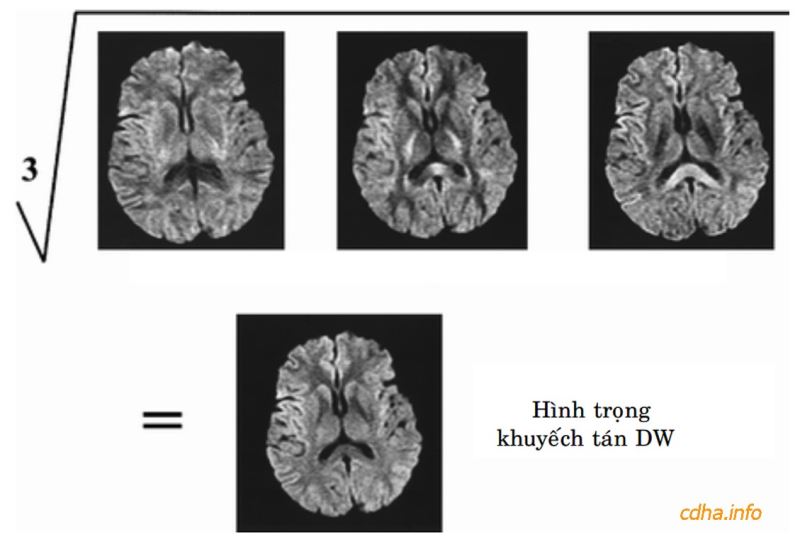
Hình 14: Hình trọng khuếch tán DW thu được từ ba hình trọng khuếch tán được chụp theo ba trục không gian đã được minh họa trong Hình 13.
- Các hình bản đồ ADC (ADC map) biểu thị độ lớn thuần túy của hệ số khuếch tán biểu kiến ADC, không có yếu tố tương phản trọng Chúng có thể được tính ra từ hình trọng khuếch tán DW và hình trọng T2 đã được chụp với giá trị b = 0. Với đặc điểm này, hình bản đồ ADC cho phép loại trừ các đặc thù trọng T2 “ăn theo” vốn có thể biểu hiện trên hình trọng khuếch tán DW.
Cho đến thời điểm hiện nay, các hình khuếch tán mặc dù đã khá thông dụng nhưng các ứng dụng chủ yếu của chúng vẫn là các ứng dụng trong lĩnh vực thần kinh. Trong trường hợp đột quỵ đến sớm (dưới 6 giờ) do nguyên nhân tắc mạch, chúng hầu như là nguồn thông tin duy nhất giúp chúng ta xác định xem vùng mô não bị thiếu máu hiện tại còn sống hay không. Thông tin này cho phép các bác sỹ lâm sàng có đủ cơ sở để đưa ra các quyết định điều trị thích hợp (Hình 15).
Cũng cần nói thêm rằng trong các hình trọng khuếch tán DW, vùng mô có hiện tượng khuếch tán kém sẽ có tín hiệu cao (trắng hơn). Ngược lại trong các hình bản đồ ADC vốn là hình biểu thị độ lớn của hệ số khuếch tán biểu kiến ADC, vùng mô kém khuếch tán (ADC nhỏ) sẽ có tín hiệu thấp (đen hơn).
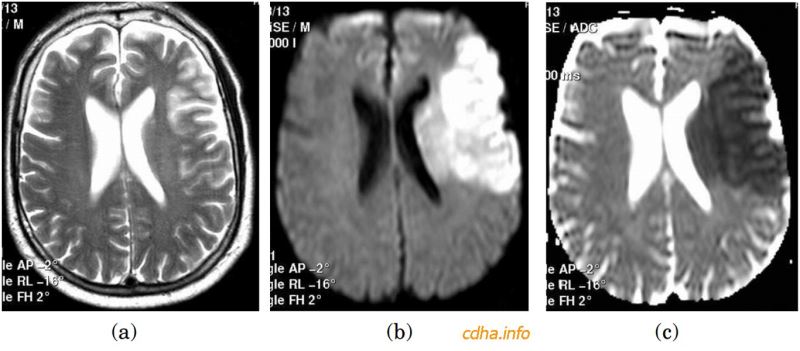
Hình 15: Nhồi máu cấp đến sớm trước 6 giờ. (a) Hình trọng T2 chỉ thấy tăng nhẹ tín hiệu ở vùng thùy đảo bên trái. (b) Hình trọng khuếch tán DW cho thấy tăng tín hiệu điển hình của vùng cấp máu từ động mạch não giữa trái. (b) Hình bản đồ ADC có giảm tín hiệu rõ ở vùng này.
6. Nguyên lý cộng hưởng từ tưới máu
Mọi cơ quan trong cơ thể đều cần dưỡng khí và chất dinh dưỡng do máu cung cấp. Hoạt động chức năng càng nhiều, lượng máu đến nuôi càng lớn. Do vậy đánh giá và lượng hóa tình trạng tưới máu (perfusion) của một vùng cơ thể thông qua các chỉ số huyết động giúp chúng ta đánh giá được mức độ hoạt động chức năng đang thực sự xảy ra tại vùng cơ thể đó. Các chỉ số huyết động thường dùng là: thể tích máu trong mô (tissue blood volume), lượng máu chảy qua mô (tissue blood flow) hay thời gian quá cảnh (transit time).
Để thực hiện điều này, người ta cần dùng một chất đánh dấu nào đó có mặt trong máu và có thể nhận ra được bằng các kỹ thuật cộng hưởng từ. Nhìn chung có hai phương pháp: phương pháp dùng chất ngoại sinh và phương pháp dùng chất nội sinh.
6.1. Phương pháp ngoại sinh
Trong phương pháp dùng chất ngoại sinh (exogenous material), người ta sử dụng một chất tương phản từ (ngoại sinh) tiêm vào cơ thể theo đường tĩnh mạch. Chúng ta biết rằng thuốc tương phản từ ngoại bào có tác dụng làm giảm cả thời gian T1 lẫn T2. Khi có mặt trong hệ thống mạch máu với một nồng độ cao, tác dụng làm giảm T2 của chúng khá rõ rệt, biểu hiện bằng sự suy giảm tín hiệu ở những vùng có tình trạng tưới máu tốt. Những vùng chậm suy giảm tín hiệu được xem như có tình trạng tưới máu kém hơn (đánh giá định tính).
Cách làm thông dụng là bơm dồn (bolus), nghĩa là bơm một lượng thuốc thật nhiều và thật nhanh vào tĩnh mạch rồi dùng một kỹ thuật chụp nhanh như chuỗi xung đồng phẳng EPI để ghi nhận sự thay đổi tín hiệu vốn xảy ra rất nhanh ở các mô cần đánh giá khi thuốc tương phản lần đầu chảy qua vùng mô đó. Ở não, thời gian chụp toàn bộ não thường chỉ dưới 2 giây.
Từ dữ liệu về sự thay đổi tín hiệu theo thời gian, người ta sẽ biến đổi thành dữ liệu về nồng độ tương đối của thuốc có trong mô theo thời gian. Những dữ liệu này cuối cùng sẽ được tính toán để quy thành các chỉ số huyết động (đánh giá định lượng). Quá trình tính toán này hiện nay đều do máy tính thực hiện nên chúng ta không bàn sâu ở đây. Kết quả có thể được hiển thị dưới dạng các bản đồ tưới máu và có thể được mã hóa bằng các màu sắc khác nhau, biểu thị các giá trị huyết động khác nhau cho từng vùng.
6.2. Phương pháp nội sinh
Trong phương pháp này, người ta sử dụng các kỹ thuật cộng hưởng từ để đánh dấu trực tiếp lên các proton trong máu trước khi chúng chảy vào vùng khảo sát. Cụ thể, người ta có thể dùng một xung bão hòa hoặc xung đảo nghịch 180o để “đánh dấu” các proton. Do đã bị đánh dấu (bão hòa hoặc đảo nghịch), dòng máu có chứa các proton này khi chảy vào vùng khảo sát sẽ làm giảm tín hiệu của vùng đó. Sự khác biệt tín hiệu khi so với hình gốc, nghĩa là hình chụp khi chưa đánh dấu, phản ánh tình trạng tưới máu của vùng đang được khảo sát.
7. Những điểm cần ghi nhớ
Những nguyên lý được phân tích trong phần này phần lớn đã được bàn luận khá chi tiết ở những phần trước, ngoại trừ nguyên lý trọng khuếch tán và trọng tưới máu. Do vậy chúng ta chỉ nhắc lại những điểm quan trọng cần nhớ đối với hai nguyên lý này.
- Hiện tượng khuếch tán xảy ra do chuyển động Brown của các phân tử khí hoặc lỏng, nghĩa là chuyển động tự do và ngẫu nhiên theo mọi hướng. Mức độ khuếch tán của một chất ở một nhiệt độ nhất định được biểu hiện bằng hệ số khuếch tán.
- Do những đặc điểm về cấu trúc vi thể, các phân tử nước trong cơ thể khuếch tán không đồng đều theo mọi hướng. Chẳng hạn với cấu trúc của hệ thần kinh, hiện tượng khuếch tán xảy ra mạnh hơn dọc theo đường đi của các bó chất trắng. Để có thể biểu thị cả độ lớn lẫn chiều hướng khuếch tán, thay vì sử dụng hệ số khuếch tán thông thường, người ta sử dụng một hệ số đặc biệt hơn gọi là hệ số khuếch tán biểu kiến ADC.
- Để đánh giá được mức độ khuếch tán, chúng ta phải dùng các thang từ đặc biệt hơn, cho phép bộc lộ tình trạng lệch pha do ảnh hưởng của khuếch tá Các thang từ khuếch tán này được điều chỉnh bằng một tham số gọi là hệ số nhạy cảm khuếch tán b. Giá trị b = 0 cho biết ảnh chụp không nhạy với khuếch tán, nghĩa là ảnh bình thường. Giá trị b nằm trong khoảng 500 đến 1500 thường được sử dụng để đánh giá khả năng khuếch tán trong lâm sàng.
- Bộ hình khuếch tán điển hình gồm có một hình trọng T2, một hình trọng khuếch tán DW và một hình bản đồ Bản đồ ADC là hình được vẽ lại từ các giá trị ADC của các mô, do vậy vùng kém khuếch tán sẽ có màu đen hơn vùng khuếch tán tốt. Ngược lại, hình trọng khuếch tán DW ghi nhận tín hiệu của các proton trong quá trình khuếch tán của chúng tuy vẫn bị chứa một phần đặc thù trọng T2. Do vậy vùng có tín hiệu cao trên hình trọng khuếch tán DW là vùng giảm mức độ khuếch tán, ngược lại với hình bản đồ ADC.
- Tình trạng tưới máu tại các mô biểu thị cho hoạt động chức năng của mô: lượng máu đến mô càng nhiều, hoạt động chức năng càng mạnh. Lượng máu đến mô có thể đánh giá được bằng cách dùng một chất đánh dấu nào đó mà chúng ta có thể “đo được” bằng các kỹ thuật cộng hưởng từ.
- Chất đánh dấu “ngoại sinh” thường dùng là một loại thuốc tương phản từ. Chúng được bơm thật nhiều và nhanh vào tĩnh mạch, nhanh chóng làm thay đổi tình trạng từ hóa tại các mô. Khi dùng các kỹ thuật chụp thật nhanh, chúng ta có thể “đo được” sự thay đổi này.
- Chất đánh dấu “nội sinh” chính là các proton đang có mặt trong dòng máu chả Chúng được đánh dấu từ tính trước khi chảy vào vùng mô cần khảo sát bằng một phương pháp nào đó, chẳng hạn như bão hòa hoặc đảo nghịch nó. Nhờ đó khi chảy vào vùng mô đang được khảo sát, chúng có thể được nhận ra bằng các kỹ thuật chụp cộng hưởng từ.