Các yếu tố ảnh hưởng đến kết quả xét nghiệm huyết học, hóa sinh và vi sinh học
Với sự tiến bộ khoa học kỹ thuật, đặc biệt khoa học y học, nhiều kỹ thuật xét nghiệm, phân tích các thành phần các chất trong cơ thể (liên quan đến xét nghiệm huyết học, sinh hóa và vi sinh cả máu, dịch sinh học và nước tiểu, dịch não tủy,…) cho kết quả rất nhanh, chính xác và đặc biệt sẽ là cơ sở dữ liệu cùng với các dấu chứng và triệu chứng lâm sàng qua thăm khám của bác sĩ giúp cho các thầy thuốc lâm sàng chẩn đoán chính xác và điều trị cũng như theo dõi điều trị hiệu quả. Tuy nhiên, không phải lúc nào kết quả xét nghiệm cũng đi thuận chiểu với bệnh (có nghĩa là có thể dương tính giả, âm tính giả,…hoặc sai lệch rất nhiều). Điều đó có thể có nhiều yếu tố tác động và làm ảnh hưởng lên kết quả xét nghiệm từ nhiều phía: bệnh nhân - thầy thuốc - thủ thuật cận lâm sàng. Để hạn chế những sai sót và sai số trong xét nghiệm vi sinh, hóa sinh và huyết học chúng tôi - trong phạm vi bài viết này, chúng tôi trình bày một số điểm cần lưu ý khi thực hiện xét nghiệm để kết quả mang lại phù hợp nhất.
1. Những điểm cần lưu ý khi thực hiện xét nghiệm chung
Những xét nghiệm chịu ảnh hưởng của điều kiện sinh học của bệnh nhân, kỹ thuật xét nghiệm, quy trình thao tác kỹ thuật của cán bộ xét nghiệm. Do vậy, những quy chế kiểm tra chất lượng trước xét nghiệm (Pre-analytical control) vô cùng quan trong chứ không nhất thiết là trong và sau xét nghiệm. Việc kiểm tra một quy trình xét nghiệm phù hợp từ khâu lấy bệnh phẩm đến khi đọc kết quả phải thận trọng và chú ý:
1.1. Phần hành chính: khi lấy bệnh phẩm phải kiểm tra, đối chiếu đúng: họ tên, chữ lót, tuổi, giới tính, địa chỉ, số giường, số phòng bệnh, khoa phòng nào? người chỉ định xét nghiệm? Người thực hiện xét nghiệm (nếu có trước đó), lấy máu tĩnh mạch hay mao mạch, động mạch? Giờ lấy bệnh phẩm, ngày lấy bệnh phẩm.
1.2. Xác định được độ nhạy và độ đặc hiệu: luôn luôn chúng ta phải xét đến Se và Sp để chọn lựa xét nghiệm cho cùng thông số sinh hoá, mục đích đáng tin cậy và nhanh chóng, tỷ lệ nhiễu thấp nhất đem đến cho kết quả xét nghiệm (spectrum bias).
2. Các yếu tố ảnh hưởng đến quá trình lấy mẫu
Để kết quả xét nghiệm chính xác thì việc đảm bảo tuân thủ các yêu cầu trong quá trình lấy mẫu là rất quan trọng. Các điều sau đây có thể xảy ra trong quá trình lấy mẫu:
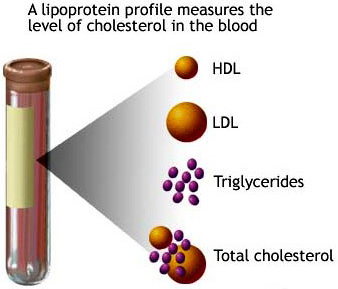
- Sau khi ăn, nồng độ các chất glucose, cholesterol, triglycerid, các acid amin, sắt và phosphate tăng lên trong máu.
- Sự thay đổi tư thế bệnh nhân đột ngột khi lấy máu có thể ảnh hưởng đến nồng độ các huyết cầu và các đại phân tử như các bạch cầu, hồng cầu, hemoglobin, hematocrit, protein toàn phần, các enzym, các lipoprotein và các ion gắn protein (như calci, sắt, …).
- Một số thuốc đang được bệnh nhân sử dụng có thể ảnh hưởng đến kết quả một số xét nghiệm sin hóa máu.
- Việc sử dụng một lượng lớn rượu trong một thời gian dài có thể làm tăng hoạt độ enzym gamma glutamyl transferase (GGT) và thể tích trung bình huyết cầu (mean corpuscular volume: MCV).
- Những người hút thuốc lá có nồng độ HbCO (carbohemoglobin) và CEA (carcinoembryonic antigen: kháng nguyên ung thư phôi) tăng.
- Giá trị một số chất có thể thay đổi trong ngày, ví dụ như các hormon (epinephrine, norepinephrine, aldosterone, corticotrophin, cortisol, prolactine, somatotropine, testosterone), các chất điện giải trong nước tiểu, nồng độ hemoglobin và sắt trong huyết thanh.
- Các bệnh nhân được làm nghiệm pháp sẽ được chuẩn bị theo yêu cầu cụ thể của từng nghiệm pháp.
- Việc lấy mẫu phải luôn được thực hiện trong những điều kiện chuẩn, nghĩa là khi bệnh nhân đói, với cùng một tư thế (ngồi hoặc nằm nghiêng), trong khoảng cùng thời gian trong ngày và sau khi buộc garô.
3. Các yếu tố có thể ảnh hưởng lên kết quả xét nghiệm máu
3.1. Lấy mẫu máu làm xét nghiệm (specimen collection).
Là bước đầu tiên, nếu lấy bệnh phẩm sai sẽ dẫn đến sai số trầm trọng cho kết quả. Lấy máu nên để nhân viên chuyên trách của phòng xét nghiệm làm, lấy máu ở hệ máu nào (tĩnh mạch, động mạch hoặc mao mạch) vì một số thông số khác nhau giữa 3 hệ này như khí máu, glucose máu, protein máu mao mạch cao hơn so với máu tĩnh mạch (do chuyển hoá, do phân bố khác nhau ở các khu vực).
3.2. Lấy máu mao mạch (dái tai, đầu ngón tay, ngón chân, hoặc ở 2 phía của gan bàn chân).
Khi cần một thể tích nhỏ máu ở trẻ sơ sinh và trẻ em, để tránh sai số do sự hoà loãng khi lấy máu mao mạch thì phải đảm bảo cho máu chảy tự do, không nặn bóp vị trí lấy máu.
3.3. Thời gian buộc garot
Thường buộc garot ở vị trí lấy máu tĩnh mạch, sự cô máu trong thời gian 3 phút sau khi buộc garot cao hơn so với thời điểm 1 phút. Tại thời điểm 3 phút, sự ứ đọng máu làm tăng sự phân huỷ yếm khí glucose máu và làm giảm pH máu cùng sự tích tụ của latate.
Hiện tượng thiếu oxy dẫn đến giải phóng K+ từ tế bào. Có sự tăng nồng độ ion Ca++ và Mg++ ở máu trong thời gian buộc garot. Tốt nhất là tháo garot ngay sau khi kim đã vào tĩnh mạch.
3.4. Tư thế bệnh nhân khi lấy máu
Nằm hay đứng có thể thay đổi một số nồng độ các chất trong máu. Khi lấy máu nên để bệnh nhân ngồi nghỉ khoảng chừng 10 phút trước khi lấy máu xét nghiệm.
3.5. Thời gián lấy máu
Sự thay đổi sinh học ngày đêm hoặc theo chu kỳ tháng (kinh nguyệt) của một số chất trong máu, nên nồng độ có thể thay đổi khi lấy máu (VD: nồng độ cortison cao nhất 6-8 giờ sáng, giảm dần buổi chiều hay nửa đêm, dung nạp glucose cũng cao hơn ở buổi chiều so với buổi sáng, sự bài tiết hormone GH thấp ở thời gian thức).
3.6. Thời gian nhịn ăn trước khi lấy máu
Thời gian nhịn ăn kéo dài 48 giờ làm tăng nồng độ bilirubine huyết thanh và giảm nồng độ albumin, pre-albumine, transferrine.
Nên lấy máu ở thời gian đói qua đêm, ít nhất là 12 giờ trước khi lấy máu vì nồng độ triglyceride có thể bị ảnh hưởng bởi bữa ăn ở thơì điểm 9 giờ trước khi lấy máu.
3.7. Chất chống đông và chất bảo quản
- Chất ức chế phân huỷ glucose máu như fluor cần thiết cho sự bảo quản máu (ngoại trừ trường hợp huyết tương hay huyết thanh cần tách ra khỏi tế bào, nếu máu để định lượng glucose mà không có chất bảo quản sẽ giảm chất lượng khoảng 7% trong giờ đầu sau khi lấy máu.
- Trì hoãn việc tách hồng cầu khỏi huyết thanh sẽ làm cho thành phần hồng cầu thoát ra huyết thanh hay huyết tương (đặc biệt trong xét nghiệm kali máu).
- Heparin nước có thể gây sai số do pha loãng mẫu máu, điều này có thể khắc phục bằng cách làm đông khô heparin trong bơm tiêm.
- Chất chống đông EDTA (Ethylen Diamin Tetra Acetat) tốt nhất là Di-potassium EDTA, thường dùng lấy máu làm xét nghiệm huyết học, nhưng không dùng để lấy máu định lượng calci, kali. EDTA là chất chống đông lý tưởng để ổn định lipid vì nó ngăn sự oxy hoá lipid nhờ phản ứng tạo phức hợp chelat hoá.
3.8. Thời gian lưu giữ máu
Thời gian lưu trữ có khả năng làm thay đổi một số chất trong máu, VD: máu dùng để đo khí máu, pH nếu không giữ được trong nước đá (0 - 40C) sẽ bị giảm chất lượng đáng kể trong vòng 15phút. Nếu được cất trong ngăn đá sẽ giúp tránh giảm chất lượng đi 10 lần.
3.9. Sự tan huyết
Do lấy máu không tốt, làm tăng các thành phần của hồng cầu (kali, phospho, ..) trong huyết thanh hay huyết tương và tăng hemoglobin. Hemoglobin có thể gây nhiễu trong một vài phương pháp xét nghiệm liên quan đến đọ hấp thụ bước sóng.
3.10. Tác dụng của việc tiêm truyền
Nếu đang truyền glucose trên tay cùng tay lấy máu thì sẽ cho kết quả glucose máu tăng cao.
4. Biến đổi thông số xét nghiệm do nguồn gốc sinh lý
4.1. Giới tính
Nồng độ một số chất trong máu và nước tiểu có sự khác nhau giữa nam và nữ (nồng độ Hb nữ < nam, các hormone sinh dục, glucose, phosphatase kiềm, ure, creatinin, hormone giáp trạng).
4.2. Tuổi
Trẻ sơ sinh và người trưởng thành khác nhau rõ rệt (bilirubine, cholesterol, ure, creatinin..), nếu chúng ta không chú ý, đôi khi đưa đến biện luận chẩn đoán nhầm dựa trên đơn thuần xét nghiệm. Nồng độ một số chất có thay đổi giữa người trưởng thành và người cao tuổi (creatinin, ure, phosphatase kiềm, hormone sinh dục, một số chỉ điểm khối u, cholesterol).
4.3. Chế độ ăn và tập quán
- Nồng độ một số chất như triglyceride (sau ăn nhiều mỡ), GGT (tăng sau khi uống nhiều rượu), phosphat và canxi huyết thanh (sau khi uống nhiều sữa).
- Rượu: ở một số người nghiện rượu nặng, sẽ có sự thay đổi hoạt độ một số enzyme SGOT, SGPT, GGT.
- Hút thuốc lá: do thuốc lá có ái lực cao với Hb nên các thành phần trong thuốc lá như CO, CO2 sẽ gây MetHb.
- Cà phê: ức chế phosphodiester (một enzyme phân huỷ AMPc thành 5’ AMP), quá trình phân huỷ glucose và lipide tăng lên, acide béo tự do huyết tương tăng gấp 3 lần.
- Thói quen luyện tập thể dục: thay đổi hoạt động enzyme của cơ: creatin phosphokinase (CK) cũng như SGPT, tăng rõ sau luyện tập thể dục, hoặc nó cũng tăng lên ở những bệnh nhân sau nhồi máu cơ tim. Hemoglobine niệu có thể tăng lên sau luyện tập nặng,gây hiện tượng tán huyết.
4.4. Thuốc điều trị đang sử dụng
- Thực tế như chúng ta đã biết thường bệnh nhân đến với chúng ta khi bệnh đã chuyển nặng hay dùng thuốc không khỏi, nên chúng ta cũng khó tránh khỏi sự nhiễu kết quả xét nghiệm. Nên cán bộ xét nghiệm cũng nên nắm một số thuốc có thể ảnh hưởng két quả, để loại trừ.
- Thuốc lợi tiểu thiazide ảnh hưởng lên kết quả xét nghiệm huyết thanh.
- Thuốc tránh thai làm thay đổi một số nồng độ protein gắn hormone.
- Paracetamol, nhóm salicylate ảnh hưởng đến một số màng điện cực chọn lọc ion (tác dụng nhiễu kết quả giai đoạn trước xét nghiệm).
4.5. Những sai số kỹ thuật được ứng dụng trong sinh hoá
- Sai số ngẫu nhiên (random error): xảy ra một cách ngẫu nhiên khó thể tránh khỏi, có thể do nhiều nguyên nhân (thuốc thử hỏng, dụng cụ đo lường không chính xác, dòng điện không ổn định, thao tác người làm xét nghiệm, thiết bị không chuẩn.
- Sai số hệ thống (systemic error): do chất lượng thuốc thử kém, chuẩn sai, kỹ thuật xét nghiệm không đặc hiệu. Nó dẫn đến sự dịch chuyển của các kết quả xét nghiệm theo cùng một hướng.
- Sai số bất thường (gross error): có thể tránh được, tần xuất sai số tuỳ thuộc vào chất lượng người làm xét nghiệm và vài yếu tố ảnh hưởng từ ngoaị cảnh: vệ sinh, trật tự, thông gió, tiếng ồn.
Các sai số trên khác biệt với OLR (Odds-likelihood ratios) để tính toán khả năng/ tần suất mắc bệnh sau cùng.
5. Một số điểm chú ý trước khi thực hiện xét nghiệm
5.1. Các yếu tố ảnh hưởng đến quá trình lấy mẫu
- Sau khi ăn, nồng độ các chất glucose, cholesterol, triglycerid, các acid amin, sắt và phosphate tăng lên trong máu.
- Bệnh nhân thay đổi tư thế đột ngột khi lấy máu có thể ảnh hưởng đến nồng độ các huyết cầu và các đại phân tử như các bạch cầu, hồng cầu, hemoglobin, hematocrit, protein toàn phần, các enzym, các lipoprotein và các ion gắn protein (như calci, sắt,...).
- Sử dụng một số thuốc có thể ảnh hưởng đến kết quả một số xét nghiệm.
- Sử dụng một lượng lớn rượu trong một thời gian dài có thể làm tăng hoạt độ enzym gamma glutamyl transferase (GGT) và thể tích trung bình huyết cầu (mean corpuscular volume: MCV).
- Những người hút thuốc lá có nồng độ HbCO (carbohemoglobin) và CEA (carcino-embryonic antigen) kháng nguyên ung thư phôi tăng.
- Giá trị một số chất có thể thay đổi trong ngày như: các hormon, ví dụ như: epinephrine, norepinephrine, aldosterone, corticotrophin, cortisol, prolactin, somatotropin và testosterone; các chất điện giải trong nước tiểu, nồng độ hemoglobin và sắt trong huyết thanh.
- Cần lưu ý khi bệnh nhân được làm nghiệm pháp sẽ chuẩn bị tùy theo yêu cầu cụ thể của từng nghiệm pháp.
5.2. Quá trình thu lượm mẫu
- Các xét nghiệm hoá sinh lâm sàng hầu hết được thực hiện với huyết thanh, huyết tương hoặc máu toàn phần.
- Máu thường được lấy vào buổi sáng, khi bệnh nhân chưa ăn uống (có những xét nghiệm không cần nhịn ăn (theo chỉ dẫn của xét nghiệm viên).
5.2.1. Huyết thanh
Huyết thanh thu được bằng cách để máu đông tự nhiên trong khoảng thời gian từ 30 phút đến 1 giờ, ly tâm ở khoảng 3.000 vòng/ phút trong 10 phút, phần dịch nổi (supernatant) phía trên là huyết thanh.
5.2.2. Huyết tương
Huyết tương thu được khi loại ion Ca2+ trong máu bằng cách thêm vào máu chất chống đông là các chất tạo phức (chelators) để tạo phức với ion Ca2+ như EDTA, citrat, oxalate hoặc heparinat.
- EDTA-K2 và EDTA-K3 với nồng độ 1,5-2 mg/ml máu được sử dụng cho các xét nghiệm huyết học thông thường.
- Heparine dưới dạng các muối như amon, Li, Na, K được sử dụng theo tỷ lệ 25U/ml máu, hay 0,01-0,1 ml heparin/ml máu.
- Fluoride (muối Na) được sử dụng với nồng độ 2 mg/ml máu. Fluoride có tác dụng cản trở sự đông máu và sự đường phân (glycolysis), nên thường được sử dụng để định lượng glucose máu.
- Dung dịch citrat (muối Na) nồng độ 3,8% hoặc 0,11 mol/L được sử dụng cho các xét nghiệm đông máu với tỷ lệ 1 thể tích Na citrate và 9 thể tích máu toàn phần hoặc được sử dụng để lắng hồng cầu với tỷ lệ 1 phần Na citrate và 4 thể tích máu toàn phần.
- Kali oxalate ít khi được sử dụng chống đông máu để lấy huyết tương.
Sau khi chống đông, ly tâm khoảng 3.000 vòng/phút trong 10 phút, dịch nổi phía trên thu được là huyết tương. Sự khác nhau giữa huyết thanh và huyết tương thường chỉ thấy trong sự xác định K+, phosphate vô cơ, lactate dehydrogenase (LDH) và điện di fibrinogen.
Ở các bệnh nhân bị chứng tăng tiểu cầu (thrombocytosis), giá trị tiểu cầu vượt trên 800.000/μL (hoặc Giga/L), việc định lượng K+ không thể thực hiện được trong huyết thanh, cần phải sử dụng thay thế bằng huyết tương chống đông với heparin.
5.2.3. Cách thu lượm máu toàn phần
Máu toàn phần có thể thu được bằng cách sử dụng các chất chống đông như đã nêu trên (không ly tâm). Một số xét nghiệm đòi hỏi sử dụng các chất chống đông khác nhau, chẳng hạn:
- Thu lượm máu để định lượng glucose máu: vì tốc độ đường phân (glycolysis) là khoảng 7% mỗi giờ nên cần phải thêm một chất ức chế quá trình đường phân, như NaF (sodium fluoride) hoặc iodoacetate vào mẫu máu trước khi xác định nồng độ glucose máu.
- Thu lượm máu để xét nghiệm huyết học: phần lớn các phân tích về huyết học, người ta thường sử dụng máu tĩnh mạch chống đông bằng EDTA. Trong trường hợp riêng biệt, sự giảm tiểu cầu giả (pseudothrombopenia) cảm ứng bởi EDTA có thế xảy ra, mặc dù điều này không có ý nghĩa lâm sàng. Việc sử dụng máu chống đông bằng citrat sẽ làm số lượng tiểu cầu trở về bình thường.
- Thu lượm máu để xét nghiệm đông máu: trong các xét nghiệm đông máu, huyết tương chống đông bằng citrat được sử dụng cho các mục đích phân tích. Cần phải trộn dung dịch Na citrat vào máu chính xác theo tỷ lệ là 1 thể tích Na citrat 3,8% và 9 thể tích máu toàn phần.
- Chú ý, máu chống đông bằng hợp chất EDTA hoặc axalat không sử dụng được cho các xét nghiệm về đông máu. Phải loại bỏ các mẫu máu bị tan huyết hoặc bắt đầu đông máu.
5.2.4. Thu lượm nước tiểu
Khi phân tích nước tiểu cần phải chú ý:
- Có một sự khác nhau rõ rệt trong ngày về sự bài tiết của một số chất, ví dụ, nước tiểu phải được xử lý trước để ổn định các catecholamin và cần phải thu lượm tất cả nước tiểu bài tiết trong thời gian quy định.
- Để xác định calci, toàn bộ lượng nước tiểu trong 24 giờ phải được acid hoá và được đun nóng.
5.2.5. Thu lượm dịch não tuỷ (cerebrospinal fluid: CSF)
- Dịch não tuỷ được thu lượm để phân tích hoá sinh lâm sàng phải được xử lý với EDTA;
- Để ngăn ngừa sự hình thành cục đông fibrin, tránh cho việc làm sai lạc số lượng tế bào đếm được.
5.3. Cách bảo quản và vận chuyển các mẫu xét nghiệm
- Việc ly tâm thường được thực hiện trong khoảng 1 giờ sau khi mẫu được thu lượm.
- Nếu các mẫu được gửi đi, chỉ được sử dụng huyết thanh hoặc huyết tương, trừ trường hợp thật đặc biệt, máu toàn phần mới được vận chuyển đi xa để phân tích.
- Vì vậy, trong mỗi loại xét nghiệm cần phải có cách bảo quản khác nhau:
5.3.1. Bảo quản các enzym
- Các mẫu huyết tương sử dụng để đo hoạt độ enzym nói chung, thường có thể bảo quản ở 40C đến 5 ngày mà hoạt độ enzym không giảm quá 10%.
- Riêng đối với LDH, không bảo quản trong tủ lạnh vì hoạt độ của nó giảm khi các isoenzym LDH4 và LDH5 của nó không ổn định trong điều kiện lạnh.
- Còn ACP chỉ ổn định khi mẫu huyết tương được acid hoá.
5.3.2. Bảo quản các cơ chất
- Các chất chuyển hoá trong huyết tương thường ổn định ở 40C trong 6 ngày mà nồng độ không có sự thay đổi đáng kể. Riêng đối với triglycerid có thể bị giảm do bị lipase thuỷ phân. Tuy nhiên, nồng độ này không thay đổi nếu phương pháp phân tích qua glycerol toàn phần.
- Nếu sự xác định dựa trên phản ứng Jaffé thì bảo quản ở nhiệt độ phòng có thể làm giảm nồng độ của phosphat, acid uric và creatinin.
- Bilirubin bị phá huỷ khi bị ánh sáng chiếu vào trong quá trình bảo quản. Glucose sẽ chỉ được bảo quản sau khi tách protein khỏi mẫu máu hoặc thêm chất ổn định.
5.3.3. Bảo quản các protein, các kháng nguyên và kháng thể
Các protein, các kháng nguyên và kháng thể được bảo quản ở 4oC trong 1 tuần.
5.3.4. Bảo quản các hormon và dấu ấn ung thư
- Các hormon steroid tương đối bền, có thể bảo quản ở nhiệt độ phòng (25oC) trong 3 ngày; các dấu ấn ung thư cũng có thể bảo quản như vậy.
- Các hormon peptid, đặc biệt là các hormon không bền là ACTH, renin, insulin, GH và calcitonin muốn bảo quản quá 1 ngày phải để vào tủ lạnh sâu.
5.3.5. Bảo quản mẫu để xét nghiệm các chất đông máu
- Huyết tương nghèo tiểu cầu sử dụng để xác định thời gian prothrombin không được để quá 8 giờ.
- Hoạt độ của các chất đông máu phải được xác định trong khoảng 3 giờ, nếu quá thời hạn trên, huyết tương phải được bảo quản ở 4oC.
5.3.6. Bảo quản mẫu làm tổng phân tích máu
Mẫu máu toàn phần chống đông bằng EDTA chỉ được sử dụng dưới 24 giờ.
5.3.7. Bảo quản mẫu để phân tích hình thái tế bào máu
- Sự dàn máu trên phiến kính chỉ được thực hiện trong vòng 5 giờ sau khi lấy máu.
- Nếu sử dụng máu để phân tích các thành phần của máu, mẫu máu được sử dụng không quá 8 giờ.
5.3.8. Bảo quản mẫu trong một thời gian dài
- Nếu muốn bảo quản bệnh phẩm trong thời gian dài hơn thời gian nêu trên, bệnh phẩm cần được bảo quản ở nhiệt độ thấp hơn -200C.
- Khi cần sử dụng, mẫu cần được tan đông một cách từ từ ở 4-80C qua một đêm hoặc trong một bể điều nhiệt có lắc.
- Tuy nhiên, việc đông băng và tan đông không nên lặp đi, lặp lại.
5.3.9. Bảo quản nước tiểu để xét nghiệm cặn nước tiểu
- Cặn nước tiểu phải được đánh giá trong khoảng 2 đến 3 giờ.
- Không được bảo quản mẫu nước tiểu trong tủ lạnh hoặc đông băng vì điều kiện lạnh có thể gây kết tủa muối.
5.3.10. Bảo quản dịch não tuỷ
Việc đếm các tế bào trong dịch não tuỷ phải được thực hiện trong vòng 1 giờ.
5.3.11. Bảo quản máu để đo khí máu và thăng bằng acid-base
5.3.12. Cách vận chuyển các mẫu xét nghiệm
- Khi chuyển bệnh phẩm từ nơi này sang nơi khác trong nước hoặc ra quốc tế, cần bảo quản bệnh phẩm trong phích đá khô.
- Nói chung, sự thay đổi hoạt độ enzym và nồng độ các chất chuyển hoá không quá ± 10% trong khoảng 2 ngày, nếu nhiệt độ bảo quản mẫu dưới 25oC.
5.4. Ảnh hưởng của tình trạng mẫu đến kết quả xét nghiệm
Mẫu máu trong điều kiện nhất định có thể ảnh hưởng đến kết quả của một số xét nghiệm:
5.4.1. Sự tan máu
- Việc xác định K+, Mg2+ hoặc LDH không thể thực hiện được ngay cả khi huyết thanh chỉ bị tan máu rất ít.
- Sự tan máu rõ ràng cũng ảnh hưởng đến các xét nghiệm khác.
- Nếu thấy mẫu bị tan máu, cần loại bỏ mẫu máu ấy và phải lấy ngay một mẫu máu mới để thay thế.
5.4.2. Bilirubin máu
- Các nồng độ bilirubin trên 5 mg/dL (86 μmol/L) ảnh hưởng đến sự xác định acid uric (phương pháp PAP).
- Các nồng độ bilirubin trên 10 mg/dL (170 μmol/L) ảnh hưởng đến sự xác định triglycerid (theo phương pháp GPO-PAP) và sự xác định creatinin (phương pháp Jaffé và PAP).
- Phương pháp xác định creatinin mới không bị ảnh hưởng của bilirubin ngay cả khi nồng độ bilirubin lên đến 25 mg/dL (430 μmol/L).
5.4.3. Sự tăng lipid máu (lipemia)
- Lipid cao trong máu có thể cản trở việc đo các chất bằng phương pháp đo quang.
- Trong trường hợp này cần loại bỏ các lipoprotein trong huyết tương bằng cách sử dụng Freon.
Tài liệu tham khảo:
1. Huỳnh Hồng Quang (2010). Bài giảng sinh hóa, Tài liệu giảng dạy trung học xét nghiệm.
2.http://www.medelab.vn. Các yếu tố ảnh hưởng lên quá trình lấy mẫu.
2. http://www.medelab.vn và medlatec.vn. Một số điểm chú ý trước khi thực hiện xét nghiệm
Nguồn: Huỳnh Hồng Quang, Nguyễn Tấn Thoa, Võ Thị Thu Trâm. http://www.impe-qn.org.vn/impe-qn/vn/portal/InfoDetail.jsp?area=58&cat=936&ID=4789